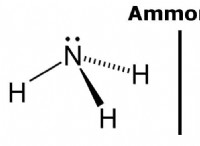
물은 지구상에서 가장 흔한 물질 중 하나 인 무색, 무취, 맛이 없으며 거의 투명한 화학 화합물입니다. 단일 물 분자는 화학적 공식 H 2 를 갖는다. o, 그것은 두 개의 수소 (H) 원자와 단일 산소 (O) 원자로 구성되어 있음을 의미합니다.
물은 분자 구조가 다른 화합물이 가지고 있지 않은 다수의 흥미로운 특성을 가지고 있다는 점에서 독특한 물질입니다. 물의 고유 한 특성 중에는 솔벤트 기능, 높은 비등 및 증발점, 높은 비열 용량, 비 압축성 및 다중 신성 특성이 있습니다.
물은 아마도 인류 역사상 가장 많이 연구되고 잘 이해 된 화합물이므로 그 특성은 오랫동안 알려져 왔습니다. 사실, 고대 그리스 자연 주의자 탈레스는 우주가 근본적으로 물이고 존재하는 모든 것이 물의 수정이라고 생각했습니다. 그것은 세 가지 물질 상태에서 자연에서 일반적으로 발견되는 유일한 물질이며, 물의 용매 능력은 우리가 알고있는 삶에 필요합니다. 인체의 60% 이상이 물로 구성되며 지구 표면의 70% 이상이 물로 덮여 있습니다. 물은 또한 다양한 측정 단위의 표준 보유자 역할을합니다. 예를 들어, 켈빈 온도 스케일은 물의 트리플 포인트를 기준으로하며 정확히 273.16 ° K로 정의됩니다.
물의 물리적 특성
극성
물은 극성 화합물이므로 전기 쌍극자 모멘트가 있음을 의미합니다. 산소 원자는 수소 원자보다 훨씬 전기 음성이기 때문에, 산소 원자는 공유 전자를 더 크게 당기는데,이 불평등 한 힘은 전자가 수소 원자보다 산소 원자를 향해 더 경향이있다. 결과적으로 물 분자는 분자의 산소 말단에 국소화 된 부분 음전하를 갖고 수소 말단에 국한된 2 개의 부분 양전하가 있습니다.
.물 분자의 극성은 물의 용매 특성을 설명합니다. 다른 극성 물질이 물에 침지 될 때, 부분적으로 하전 된 산소 및 수소 끝은 침지 된 물질에서 분자의 부분적으로 하전 된 끝을 끌어냅니다. 물 분자는 침지 된 물질의 분자를 제거하고 용해시킨다. 물은 좋은 용매이기 때문에 종종 수성 산성 용액을 만드는 데 사용됩니다.
수소 결합
물의 극성을 사용하면 수소 결합이라는 특수한 분자간 결합에 관여 할 수 있습니다. 수소 결합은 하나의 분자에서 수소 원자와 다른 분자에서 전기 음성 원자 사이에 형성되는 정전기 결합이다. 물 분자에서 산소는 부분 음전하를 갖는다. 이 부분 음전하는 다른 물 분자의 양의 수소 끝을 유치 할 것이다. 수소는 매우 작은 원자이기 때문에 인접 산소 원자에 매우 가까워 질 수 있습니다. 정전기 인력은 두 개의 하전 된 입자 사이의 거리의 제곱과 비늘이므로, 매우 가까운 수소 원자는 인접한 물 분자에서 산소 분자에 다소 강한 정전기 당김을 가해집니다. 각 물 분자는 이웃 물 분자와 4 개의 별개의 수소 결합을 형성 할 수 있습니다.
물의 수소 결합은 물의 흥미로운 물리적 특성을 설명합니다. 대부분의 화합물은 얼어 붙을 때 수축합니다. 물질에서 운동 에너지를 제거하면 구성 분자의 운동이 느려져 분자를 가깝게 유지하는 분자간 결합을 극복 할 가능성이 적습니다. 물이 냉각되면 약 4 ° C에 도달 할 때까지 예상되는 것처럼 수축합니다. 이 시점에서 물은 총 부피의 약 9% 씩 증가합니다.
수소 결합으로 인해 물이 얼리면 물이 팽창합니다. 물이 냉각되면 구성 분자가 느려집니다. 느리게 움직이는 물 분자는 다른 물 분자와 수소 결합을 형성하는 데 더 취약하다. 수소 결합의 독특한 특성은 분자를 엄격한 사면체 격자와 같은 구조로 배열합니다. 이것이 바로 얼음이 액체 물에 떠 다니는 이유입니다. 얼어 붙을 때 물이 팽창하기 때문에 얼음 샘플은 같은 질량을 가진 액체 물 샘플보다 밀도가 낮습니다.
열역학적 특성
물의 수소 결합은 여러 IT 열역학적 특성을 설명합니다. 유사한 분자 구조를 가진 다른 화합물과 비교하여, 물은 자연스럽게 높은 끓는점을 갖는다. 물질을 끓이기 위해서는 구성 분자가 분자간 결합을 극복 할 수 있도록 물질에 운동 에너지를 첨가해야합니다. 강한 수소 결합으로 인해 물 분자의 운동이 분자간 결합을 극복하기 위해서는 상대적으로 더 많은 에너지가 필요합니다.
.마찬가지로, 같은 이유로 물은 비열 용량이 매우 높습니다. 물질의 열 용량은 물질 그램의 온도를 1도 K로 높이는 데 필요한 에너지의 양입니다. 물의 비열 용량은 약 4.2 J/g⋅K이므로 순수한 물의 1 그램 온도를 1도 켈빈으로 높이려면 4.2 줄의 에너지가 필요합니다. 이 값을 황화수소와 비교하십시오 (H 2 S), 물과 같은 분자 구조를 갖는 화합물. 황화수소의 비열 용량은 1,0003 J/g⋅K입니다. 즉, 1 그램의 물 온도를 단일 수소 질량의 온도를 단일 도로 높이는 데 걸리는 양보다 1 그램의 물 온도를 단일 도로 높이려면 거의 4 배 더 많은 에너지가 필요합니다.
.또한 칼로리 열 단위는 순수한 물 그램의 온도를 1도 섭씨로 높이는 데 필요한 열 에너지의 양으로 정의되므로 켈빈과 섭씨 온도는 동일한 크기의 단위를 가지므로 1 칼로리는 4.2 줄과 같습니다.
또한, 수소 결합은 물에 높은 열의 융합, 기화 열 및 열전도도를 제공합니다. 이러한 특성의 조합은 물이 열을 전달하고 온도를 조절하는 데 매우 효율적으로 만들어집니다. 이 메커니즘은 물이 열을 저장하고 바다와 대기 사이로 운반하는 지구 기후에서 가장 분명합니다. 물의 열적 특성은 또한 산업 목적에 유용합니다. 증기 엔진 및 유압 기술은 물의 열역학적 특성을 사용하여 기계적 에너지를 생성합니다.
표면 장력
물의 수소 결합은 또한 상대적으로 높은 표면 장력을 제공합니다. 물 샘플의 표면에있는 분자는 주변 대기의 분자보다 인접한 물 분자에 더 단단히 결합합니다. 결과는 체중을 지탱할 수있는 표면을 가로 지르는 얇은 "필름"입니다. 물 스트라이더와 도마뱀과 같은 몇몇 유기체는이 높은 표면 장력을 이용하여 물 위를 걷습니다.
표면 장력 뒤에 동일한 메커니즘은 물의 모세관 작용을 설명합니다. 분자 사이의 분자간 관광 명소는 물이 중력에 직면하더라도 수직 튜브의 벽을 오르도록합니다. 몇몇 식물은 물 수송을위한이 모세관 작용에 의존합니다.
물의 종류
수소와 산소는 수많은 동위 원소를 가지고 있기 때문에, 몇 가지 알려진 동위 원소의 물이 존재한다. 대부분의 다른 종의 물은 수소의 다른 동위 원소의 결과입니다. 예를 들어, 양성자는 하나의 양성자 및 중성자가없는 수소의 동위 원소입니다. 대부분의 자연 발생 물은 수소의 양성자 동위 원소로 형성됩니다.
대조적으로, 중수소는 하나의 양성자와 하나의 중성자로 구성된 수소 동위 원소입니다. 중수소 물은 백만 분당 약 15 부의 속도로 발생합니다. 때때로 "헤비 워터"라고 불리는 중수소 수는 양성자 수보다 약간 더 거대합니다. 이 질량은 더 나은 열전도율 특성으로 해석됩니다. 따라서, 중수소는 종종 원자로에서 중성자 싱크 및 냉각수로 사용됩니다. 대량의 중수소의 인간 소비는 생물학적 합병증, 특히 신경 및 신장 장애를 유발할 수 있습니다.
또한 2 개의 중성자를 갖는 수소 원자로 만들어진 물의 동위 원소가 존재한다. "삼중 수소"물은 양성자 수와 중수소 수보다 더 방량입니다. 삼중 수수는 방사성이며 약 4,500 일의 반감기로 붕괴됩니다. 자연적으로 발생하는 삼중 수소는 우주 광선에 의해 수증기가 폭격되는 상부 대기에서 형성됩니다.
측정의 표준으로서 물
물은 어디에나 있고 그 특성이 잘 이해되기 때문에, 역사적으로 측정 단위에 대한 표준을 설정하는 데 사용되었습니다. 실제로, 매우 오랫동안, 물은 표준 질량 단위 인 그램 (g)을 정의하는 데 사용되었습니다. 1795 년에, 1 킬로그램은 1 입방 데시 리터 (10cm x 10cm x 10cm 큐브)의 질량으로 정의되었다. 1900 년에 리터 (L)는 표준 압력과 온도에서 1kg의 물량으로 정의되었습니다.
또한 섭씨 및 켈빈 온도 척도는 각각 비등점과 트리플 포인트를 기반으로합니다. 100 ° C는 압력 1 대기에서 물의 비등점으로 정의되며, 물의 트리플 포인트는 정확히 273.16 ° K로 정의됩니다. 물 1 분기 압력이 생명에 필요한 압력 13.1m 진공 컬럼에서 수압이 때때로 정의되므로 물은 표준 압력을 정의하는 데 사용되었습니다.
.마지막으로, 물은 열역학에 사용되어 열 및 열 전도도의 표준을 정의했습니다. 칼로리 (CAL)는 역사적으로 표준 온도와 압력에서 1 그램의 물 온도를 1 ° C로 높이는 데 필요한 열 에너지의 양으로 정의되었습니다.