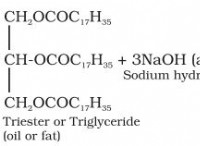1. 화학적 특성 :나트륨 원자는 안정적인 전자 구성을 달성하기 위해 가장 바깥 쪽 쉘에서 하나의 전자를 쉽게 잃게됩니다. 전자를 쉽게 포기하는이 능력은 나트륨이 전기 양성과 반응성이 높으며, 이는 금속의 특징적인 특성입니다.
2. 전자 구성 :나트륨의 원자 수는 11이므로 11 개의 양성자와 11 개의 전자가 있습니다. 나트륨의 전자 구성은 2, 8, 1으로 표현 될 수 있습니다. 가장 바깥 쪽 쉘 (n =1)은 하나의 전자 만 가지며, 이는 핵에 느슨하게 결합됩니다. 이 단일 단일 고정 된 전자를 원자가 전자라고합니다.
3. 반짝이는 외관 :대부분의 금속과 마찬가지로 나트륨은 반짝이거나 빛나는 외관을 가지고 있습니다. 이것은 자유롭게 움직일 수 있고 빛을 반사 할 수있는 유리 모바일 원자가 전자가 존재하기 때문입니다. 나트륨은 금속 광택을 제공합니다.
4. 높은 전기 전도도 :나트륨은 우수한 전기 도체입니다. 전기장이 적용되면 나트륨의 유리 원자가 전자는 금속 전체에 자유롭게 움직일 수 있으며 전류를 운반 할 수 있습니다. 이 높은 전기 전도도는 금속의 특징입니다.
5. 높은 열전도율 :나트륨은 또한 열의 좋은 도체입니다. 나트륨의 자유 이동 원자가 전자는 열 에너지를 효율적으로 전달하여 열이 금속을 통해 빠르게 흐를 수 있습니다.
6. 가용성과 연성 :나트륨은 부드럽고 가단성 금속으로 망치질이나 롤링으로 쉽게 형성 될 수 있습니다. 또한 연성이므로 파손되지 않고 얇은 와이어로 끌어들 수 있습니다. 이러한 특성은 금속 요소의 전형적인 것입니다.
7. 반응성 :나트륨은 특히 물과 반응성이 높습니다. 나트륨이 물과 접촉하면 격렬한 화학 반응을 겪고 수소 가스를 방출하고 수산화 나트륨 (NAOH)을 형성합니다. 이 반응성은 나트륨의 낮은 이온화 에너지와 원자가 전자를 잃는 경향에 기인합니다.
화학적 특성, 전자 구성, 반짝이는 외관, 전기 전도도, 열전도도, 가상성, 연성 및 반응성을 포함한 이러한 특성의 조합은 나트륨이 실제로 금속임을 분명히 나타냅니다.