일반적으로 학생들은 베이킹 소다와 소다 세척 사이에 혼란스러워집니다. 이것들은 두 가지 다른 화학 화합물의 일반적인 이름입니다. 하나는 탄산나트륨이고 다른 하나는 탄산나트륨입니다.
이제 탄산나트륨, 베이킹 소다 또는 세척 소다는 어느 쪽입니까? 이것에 대답 할 수 있습니까? 아니면 그들 사이에 혼란스러워합니까? 탄산나트륨 공식은 무엇입니까? 탄산나트륨 탄산염 공식은 무엇입니까?
이 섹션은 탄산나트륨과 그 특성과 용도에 관한 것입니다.
탄산나트륨이란 무엇입니까?
탄산나트륨은 FDA 승인 식품 첨가제입니다. 때때로 소다 재, 세척 소다, 탄산염, 탄산염 또는 소다 결정이라고도합니다. 탄산나트륨 또는 소다 재는 많은 제조 공정에서 일반적인 성분입니다.
탄산나트륨은 인위적으로 제조 될 수있는 천연 화합물입니다. 탄산나트륨은 식료품 점, 수영장 공급 상점 및 철물점에서 쉽게 구할 수 있습니다.
탄산나트륨은 중간 정도 강한 염기로 사용되는 무기 화합물입니다. 그것은 세탁 비누와 다른 많은 가정용 제품의 핵심 요소입니다.
탄산나트륨 공식 및 구조
탄산 나트륨 공식 Na로 ₃는 탄산의 단절 염입니다. 탄산나트륨 몰 질량은 106.0 g/mol입니다. 그것은 이온 성 화합물입니다. 그것은 탄산염 음이온 (Co₃⁻)과 2 개의 나트륨 양이온 (Na⁺)으로 구성됩니다. 그것은 결정질 탈 카이드 레이트 구조를 가지고 있습니다.
탄산나트륨의 구조는 다음과 같습니다.
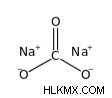
탄산나트륨의 수화물
일반적으로 탄산나트륨은 3 개의 수화물 및 무수 염 상태에 존재합니다. 이 상태는
입니다1. Natron :
탄산나트륨 데카이 드레이트입니다. 화학적 공식은 na formco₃ · 10h₂o입니다. 그것은 단일 하수물을 형성하기 위해 쉽게 결정화됩니다.
2. Thermonatrite :
탄산나트륨 모노 하이드레이트입니다. 화학적 공식은 na formco₃ · h₂o입니다. Crystal Carbonate라고도합니다.
3. 탄산 나트륨 헵타 이드 레이트 :
미네랄 형태로 알려져 있지 않습니다. 화학적 공식은 na formco₃ · 7h₂o입니다.
입니다4. 나트라이트 :
그것은 무수 탄산나트륨이며 소성 소다라고도합니다. 가열 수화물에서는 형성됩니다. 나트라이트를 얻는 또 다른 방법은 탄산나트륨을 가열하는 것입니다.
탄산나트륨의 합성
탄산나트륨 합성 과정, 즉 마이닝, Barilla 및 Kelp, Leblanc, Hou 's 및 Solvay 공정 과정이 있습니다.
이 5 가지 방법 중에서 Solvay 공정은 탄산나트륨 합성에 가장 상업적으로 사용되는 과정입니다.
Solvay 프로세스 :
벨기에의 어니스트 솔 베이 (Ernest Solvay) 산업 화학자는 1861 년에 탄산나트륨을 생산하는 방법을 개발했습니다. Solvay 프로세스에서 따르는 단계는
입니다1 단계 :탄산나트륨 생산 :
이 단계에서, 탄산나트륨 및 염화 암모늄은 암모니아, 염화나트륨 및 물을 사용하여 생산됩니다. 발생하는 화학 반응은
이었다naCl + nh n + co₂ + h₂o → nahco₃ + nh₄cl
2 단계 :탄산나트륨 생산 :
이 단계에서, 1 단계에서 나트륨 카보네이트 공식 Nahco₃를 가열함으로써, 그것은 탄산나트륨으로 변환된다. 이 단계에서는 물과 이산화탄소가 방출됩니다.
2Nahco→ → na₂co₃ + h₂o + co₂ ↑
3 단계 :재활용 암모니아 :
1 단계에서 생성 된 염화 암모늄은 석회로 처리되고, 남은 이산화탄소 생성물은 2 단계에 있습니다. 발생하는 반응은
입니다.2NH₄CL + CAO → 2NH₃ + CACL₂ + h₂O
생산 된 암모니아는 Solvay 프로세스에서 재활용됩니다. Solvay 공정에서 유일한 폐기물은 염화칼슘이며 소금물과 석회암은 유일한 소비 물질입니다. 결과적으로 프로세스는 다른 프로세스보다 실질적으로 더 경제적입니다.
탄산나트륨의 물리적 특성
환경에는 자연스럽고 인공 나트륨 탄산 나트륨이 있습니다. 당연히, 건조한 지역, 특히주기적인 호수 물이 증발 할 때 발견되는 미네랄 퇴적물에서 발생합니다.
그것은 2 곡물 솔루션 인 Trona로 만들어졌습니다. 탄산나트륨의 다른 물리적 특성은
입니다- 그것은 백색 결정질 고체 물질입니다.
- 탄산나트륨 몰 질량은 105.99 g/mol. 입니다
- 냄새가없고 맛이 없으며 물에 매우 용해됩니다.
- na로 코 ₃의 끓는점은 1600 ° C이고 851 ° C에서 분해됩니다.
- 붉은 리트머스를 파란색으로 바꾸어 기본 또는 알칼리성입니다.
- 탄산나트륨의 밀도는 2.54 g/cm³입니다.
- 그것은 몇 안되는 수용성 금속 탄산염 중 하나입니다.
- 거의 발생하지 않는 형태 중 하나를 Natrite라고합니다.
탄산나트륨의 화학적 특성
탄산나트륨의 일부 주요 화학적 특성은
입니다1. 열의 영향 :
무수 탄산나트륨에 열의 영향은 없습니다. 붕괴되지 않고 852 ° C에서 녹습니다.
2. 가수 분해 효과 :
가수 분해 동안, OH 이온이 용액으로 방출된다. 이들 이온은 탄산나트륨 용액을 약간 알칼리성으로 만듭니다.
na₂co₂ + 2h₃o → h₂co₃ + 2na⁺ + 2oh
3. 이산화탄소의 효과 :
수성 탄산나트륨은 이산화탄소를 흡수하고 탄산나트륨을 생성합니다.
na₂co₂ + h₃o + co₂ → 2nahco₃
4. 채소 산의 효과 :
라임 주스와 같은 온화한 산이 탄산나트륨과 반응하면 이산화탄소가 형성됩니다.
na₂co₂ + 2hcl → 2naCl + H₂O + Co₂
- 비누화를 통한 세제 특성이있어 지방과 기름을 뿌릴 수 있습니다.
탄산나트륨의 사용
1 . 연수 :
탄산나트륨은 Ca²⁺, mg²⁺ 및 기타 이온을 제거하여 물을 연화시킵니다. 이들 이온이 탄산염 이온으로 처리되면 불용성 고체 침전물을 형성한다. 또한 부드러운 물에는 많은 이점이 있습니다. 비누 낭비를 줄이고 파이프와 피팅의 수명을 높이고 녹에서 안전하게 유지합니다.
2. 유리 제조 :
유리 제조에는 소다 재와 가성 소다가 필요합니다. 탄산나트륨, Na로 코스는 실리카 플럭스 역할을합니다. 그것은 특수 재료없이 혼합물의 용융점을 줄이고‘소다 라임 유리’를 저렴하게 달성합니다.
3. 음식 첨가물 및 요리 :
탄산나트륨은 반사 제제, 산도 조절제, 안정제 및 양육 제로 작용하는 식품 첨가제입니다. 다양한 요리 응용 프로그램이 있습니다. 또한 맛을 향상시키기 위해 일부 식품에 추가됩니다.
4. 다른 용도 :
점토를 압제하는 데 필요한 물의 양을 줄이기 위해 벽돌 산업에서 습윤제로 사용됩니다. 많은 마른 비누 분말에는 na로 코스가 포함되어 있습니다. 또한, 그것은 거품 제로 작용하고 치약의 연마제 역할을합니다. 그것은 또한 다양한 응용 분야에서 강력한 기반으로 사용됩니다.
요약
탄산나트륨이란 무엇입니까? 요컨대, 탄산나트륨은 화학적 공식 Na로 ₃를 갖는 탄산의 단식 염입니다. 탄산나트륨 몰 질량은 105.99 g/mol입니다. 탄산나트륨을 합성하는 두 가지 방법이 있습니다.
가정뿐만 아니라 상업적으로 다양한 목적으로 유용합니다. 비누, 유리 및 기타 화학 물질을 제조하는 데 사용됩니다. 또한 pH 조정기 역할을합니다.
낮은 농도의 탄산나트륨은 피부에 해를 끼칠 수는 없지만, 수성 형태의 탄산나트륨은 반응성이 높고 부식성입니다. 심각한 피부와 눈 자극을 유발할 수 있습니다. 따라서주의와 안전으로 처리해야합니다.
자주 묻는 질문
1. 탄산나트륨 중독의 증상은 무엇입니까?
A. 소량으로 복용하면 탄산나트륨이 무해하지만 너무 많이 중독을 유발할 수 있습니다. 탄산나트륨 중독의 일부 증상에는
가 포함됩니다- 호흡 문제
- 구토
- 설사
- 저혈압
- 눈 자극
그러므로주의해서 다루십시오.
2. 탄산나트륨은 독성이 있습니까?
A. 피부와 접촉 할 때 일반적으로 무해합니다. 그러나, 탄산나트륨으로 만든 용액은 부식성이 될 수 있습니다. 소량은 독성이 없지만 너무 많이 중독을 유발할 수 있습니다. 그럼에도 불구하고, 탄산나트륨은 대부분 독성 위험이 낮습니다.
3. 탄산나트륨이 경구를 섭취하면 어떻게됩니까?
A. 탄산나트륨을 섭취하면 신체에 나트륨을 추가하지 않습니다. 섭취량조차도 음식의 나트륨 양보다 훨씬 낮습니다. 탄산 나트륨을 구두로 섭취하면 몸의 물과 혼합되어 제산제 역할을합니다. 위의 위산을 중화시킵니다. 그러나이 목적으로 일반적으로 처방되지는 않습니다.
4. 부식을 피하기 위해 식수에 탄산나트륨을 얼마나 첨가해야합니까?
A. 탄산나트륨은 종종 pH 및 알칼리도를 변화시키기 위해 일부 양으로 물에 첨가됩니다. 일반적으로 부식 제어 과정에서 1ppm ~ 40 ppm 범위에 추가됩니다. 이 금액은 음식과 음료의 자연 금액에 비해 중요하지 않습니다.
5. 탄산나트륨 제조 나트륨 제조의 Leblanc 공정에는 어떤 단계가 관여합니까?
A.이 제조 공정에서 세 단계가 진행됩니다. 이것들은
입니다1 단계 : 염화나트륨은 황산으로 처리됩니다.
2NACL + HASSOAT → NAISOAT + 2HCL
2 단계 : 황산나트륨은 석탄으로 가열됩니다.
na₂so₂ + 2c → na₂s + 2co₂
3 단계 : 황화나트륨과 탄산 칼슘 이이 마지막 단계에서 처리됩니다.
na₂s + caco + → na₂o₃ + cas
6. Solvay 프로세스와 관련된 재료는 무엇입니까?
A. Solvay 공정에 사용 된 주요 재료는 저렴하고 쉽게 구할 수 있습니다. 그들은
입니다- 소금물 또는 염화나트륨 용액 :
NaCl은 탄산나트륨 생산 중에 NA 이온을 제공합니다. 소금물은 지구상에서 풍부하게 제공됩니다. 바다와 내륙에서 쉽게 수집 할 수 있습니다.
- 석회암 또는 탄산 칼슘 :
Caco₃는 na₂o₃의 제조에서 공동 이온을 제공합니다. 광업에서 쉽게 구할 수 있습니다.
- 암모니아 :
NH주는 하버의 과정에 의해 산업적으로 만들어졌습니다. 비싸지 만 Solvay 프로세스에서 재활용 할 수 있습니다.