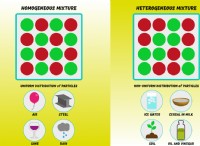
에멀젼은 분산 된 상이 불가능한 배지에 흩어져있는 액체의 미세한 글로벌로 만들어진 분산이다. 분산 매질은 분산 상이 아닌 외부 상이며, 즉 내부 단계입니다.
에멀젼을 형성하기 위해서는 유화제가 존재해야한다. 액체 에멀젼은 내용물 및 의도 된 적용에 따라 경구, 국소 또는 비경 구를 사용할 수있다. 이 기사는 유화 이론에 대한 궁극적 인 가이드와 유화 문제와 답변 이론이 될 것입니다.
유화제
에멀젼을 안정적으로 유지하기 위해 유화제가 첨가된다. 다음은 유화 특성 목록입니다.
- 그들은 친수성 (극성) 및 소수성 말단 (비극성)을 모두 갖는 화합물입니다.
- 그들은 물과 기름에 용해 될 수 있습니다
- 유화제는 분산 된 상과 배지 둘 다 사이에 층을 생성하여 분산 된 상자가 더 큰 입자를 형성하고 분리하는 것을 방지합니다 .
- 적용에 따라 양이온, 음이온 성 또는 심지어 비극성 일 수 있습니다
- 에멀젼 조성과 관련하여 물과 오일이 고려해야 할 유일한 요인은 아닙니다.
- 오일과 유화제 사이의 용해도 차이는 물이 분산제로 작용할 수 있고, 오일은 분산 상 로 작용할 수 있습니다.
- 이것은 사실 일 수 있지만, 오일이 분산 매체가 될 가능성이 높고 유화제가 오일에 수용성이있을 때 분산 된 상을 물로 물을 뿌릴 가능성이 높습니다
- 단백질, 잇몸, 비누 및 기타 전형적인 유화제는 O/W 에멀젼에 사용됩니다
셀룰로스, Datem, 계란 노른자, 겨자, 인산 나트륨, 모노 및 디 글리세리드, 인산 나트륨, 콩 레시틴 등은 유화제의 예입니다.
유화에 대한 세 가지 이론은 다음과 같습니다.
1. 표면 장력 유화 이론
- 이 이론은 표면-활성 제제가 2 개의 불가능한 액체 사이의 계면 장력을 감소시켜 액체 사이의 회전력을 감소시키고 자체 분자에 대한 각 액체의 인력을 감소 시킨다고 명시한다.
- 표면 활성제 (계면 활성제)가 사용됩니다
- 계면 활성제는 큰 지구를 작은 글로 분해하는 데 도움이되므로 다시 연결되거나 응집되는 성향이 낮아서 더 쉽게 분산시킬 수 있습니다
2. 방향 쐐기 이론 유화 이론
- 비누는 유화제가 필요하지 않고 2 ~ 4 % 오일이 물에 유화되는 희석 된 에멀젼의 일반적인 예입니다.
- 이것은 비누가 사용되면 90 번의 물이 오일에 흡수 될 수 있음을 의미합니다
- 오일-물 인터페이스에서 비누 분자의 방향 쐐기 이론 당 오일을 향한 탄화수소 급진적 지점과 Na+ 지점
- 비극성 또는 "유성"끝은 오일을 향해 회전하고 "극성"또는 "액체"끝은 극성 액체로 바뀝니다
- 방향 에멀젼 이론에 따르면, 유화제 분자의 비극성 끝이 수축 될 때 물 에멀젼의 오일 (또는 일반적인 유형)이 형성되는 반면, 극 끝이 줄어들 때 물방울이 형성됩니다
- 분자의 길 잃은 필드는 비대칭이기 때문에 유체와 고체가 내부 질량으로부터 뚜렷한 표면층을 갖기 위해서는 모든 분자가 무작위 방식으로 정렬되는 순수한 물질에있는 것과 다르게 방향을 향해야합니다.
3. 계면 필름 이론의 유화 이론
- 내부 단계방의 표면에 흡착 된 얇은 코팅은이 이론의 유화제의 액 적을 둘러싸고, 접촉 및 분산 단계의 유착을 방지합니다 >
- 수용성 화합물과 O/W와 W/O 에멀젼 사이의 직접적인 상관 관계가 있습니다
유화 이론 :중요성
몇 가지 이론은 단일 에멀젼 시스템과 관련이 있습니다. 예를 들어, 요원 형성의 초기 단계에서 계면 장력을 줄이는 것이 중요합니다. 그러나 보호 분자 쐐기 또는 유화제 층의 개발은 장기 안정성에 필수적입니다.
결론
요약하면, 표면 장력 접근법에서, 유화는 두 상 사이에 계면 장력이 감소되는 과정으로 설명된다. 계면 장력 이론에서, 유화제는 한 단계에 걸쳐 필름을 생성하여 지구의 형성으로 이어진다. 매체에 매체를 유지하기 위해이 화학 물질은 서로 저항하는 경향이 있습니다. 유화제 분자의 비극성 끝이 줄어들 때 물 에멀젼 (또는 정상 품종)의 오일이 발생합니다. 대조적으로, 방향 쐐기 가설에 따라 극단이 수축 될 때 물방울이 형성됩니다.
관련 페이지
| JEE 알림 | Jee Study 자료 |
| jee 간의 차이 | JEE 중요한 공식 |
| JEE 시험 팁 | Jee Full Forms |
| 뿌리 평균 제곱 속도 | 1 차 및 2 차 원자가 |
| Reimer-Tiemann Reaction | Arrhenius 이론의 한계 |
| 유도 성 및 메소머 효과 | 초등 및 복잡한 반응 |