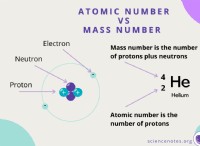
탄화수소는 수소와 탄소라고 불리는 필수 원자로 구성된 유기 화합물입니다. 일반적으로 이들은 냄새가 거의없는 무색 가스입니다. 유형에 따라 탄화수소는 단순하거나 복잡한 구조를 가질 수 있습니다. 이들은 주로 알켄, 알칸, 알킨스 및 방향족의 네 가지 주요 부분으로 분류됩니다.
탄화수소 란 무엇입니까?
탄화수소는 탄소와 수소의 두 원자를 포함하는 유기 화합물로 설명 될 수 있습니다. 탄화수소는 단순하거나 복잡 할 수있는 구조에 따라 다릅니다. 또한 포화 탄화수소, 불포화 탄화수소, 사이클로 알칸, 방향족 탄화수소, 지방족 탄화수소 및 알리 사이클리 탄화수소의 6 가지 주요 부분으로 나눌 수 있습니다.
alkynes는 무엇입니까?
유기 화학의 계열에 속하는 Alkyne 또는 Alkynes는 적어도 하나의 탄소-탄소 삼중 결합을 포함하는 불포화 탄화수소입니다. 알키네스의 공식은 CNH2N-2입니다. 삼중 결합은 또한 아세틸렌 결합이라고도합니다. Alkyne 가족에서 Ethyne은 첫 번째 회원입니다. 화학적 공식은 C2H2입니다.
알키네스의 특성
-
alkynes는 혼성화로 인해 독특합니다. 알킨의 비극성 결합 강도, 산도 및 선형성은 이들 화합물에 특징된 삼중 결합 때문이다.
-
물에있을 때,이 화합물은 불용성이지만 극성 용매에서는 약간 용해됩니다. 알킨은 용액 밀도가 적기 때문에 유기 용매에 용해되는 능력을 가지고 있습니다.
-
alkynes는 Alkanes 및 Alkenes보다 높은 비등점을 가지고 있습니다. 예를 들어, Ethane의 끓는점은 -88.6 ° C이고 Ethene의 끓는점은 -103.7 ° C이고 Ethyne의 끓는점은 -84 ° C입니다. 탄소 원자가 증가함에 따라, 이들 화합물의 끓는점도 증가한다.
-
알킨의 산도는 알칸과 알켄의 산도보다 훨씬 높습니다. 에탄의 PKA 값은 50으로, 산성이 적고, 에텐의 PKA 값은 44입니다. 반면에, Ethyne은 가장 산성이며 PKA 값은 25입니다.
알키네의 준비
alkynes를 준비하기 위해 고려되는 몇 가지 방법이 있습니다. 항균성, 항진균 및 항 기생충 특성으로 인해 알키네스의 합성은 매우 유용합니다. 다음은 Alkynes를 준비하는 데 사용되는 몇 가지 방법입니다.
알킬 디 히알리드의 탈히 할로겐화
첫 번째 방법은 알칼리가 할로겐과 반응하는 알킬 디 히알리드의 탈수소 형성입니다. 이 반응으로 인해“대체 된 알칸”이라고 불리는 또 다른 알칸이 달성됩니다. 형성된 알키네는 치환 된 알켄의 형성을 위해 알코올성 KOH를 통해 추가로 처리된다. 나중에, 그것은 나트륨 아미드와 반응하여 알킨을 형성한다. 할로겐과 함께 수소가 존재하지 않기 때문에, 공정은 탈수성 할로겐화라고한다.
여기 알킬 디 히알리드의 탈수소 형성 -
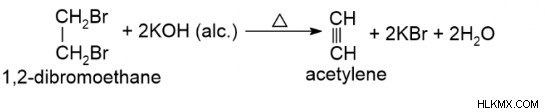
탄소 칼슘으로부터의 준비
전문가들은 Alkynes가 더 큰 규모로 생성 될 때이 방법을 선호합니다. 탄수화물의 칼슘의 화학적 공식은 CAC2입니다. 탄산 칼슘을 준비하기 위해 코크스가있는 상태에서 Quicklime을 가열합니다. 그 후, 탄수화물은 아세틸렌을 얻기 위해 물과 반응하도록 만들어진다. 탄수화물로부터 아세틸렌을 준비하기위한 반응은 다음과 같습니다 -
CACO3 → CAO + CO2
CAO + 3C → CAC2 + Co
CAC2 + 2H2O → CA (OH) 2 + C2H2
Vicinal Dihalides의 준비
이 과정에서 알켄은 할로겐과 반응합니다. 탈히 할로겐화 과정은 알키 네스를 얻기 위해 수행되며, 두 가지 주요 단계에서 수행된다.
알키 네스 제조의 첫 번째 단계는 불포화 할로이드를 준비하는 것입니다. 형성된 할라 드는 할로겐을 보유하고, 이는 이중 결합 탄소에 추가로 부착된다. 이러한 할리 드는 비닐 할리 드로 지칭된다. 이 할라이드는 본질적으로 반응하지 않지만 알킨을 형성하는 강력한 염기와 반응하도록 만들어진다. 작은 알키네를 더 큰 알킨으로 변환하기 위해, 금속 아세틸 라이드가 두 번째 단계에서 사용됩니다.
여기에 vicinal dihalides에서 알키네의 준비 -

알켄과 알칸의 차이
알켄은 탄화수소 제품군에서 나옵니다. 알켄은 적어도 두 개의 인접한 탄소 원자 사이에 하나의 이중 결합을 갖는다. 알켄의 화학적 공식은 CNH2N입니다. 알칸은 단일 결합 수소 및 탄소 화합물을 갖는 유기 화합물로 설명 될 수있다. CNH2N+2는 알칸의 공식입니다. 사이클로 알칸, 분지 알칸 및 체인 알칸의 세 가지 주요 그룹으로 나뉩니다.
Clemmensen의 축소는 무엇입니까
Clemmensen의 감소는 염산 및 아연 아말감을 사용하여 케톤 또는 알데히드를 알칸으로 줄이는 데 사용되는 반응입니다. 이 반응은 덴마크 화학자 인 Erik Christian Clemmensen의 이름을 따서 명명되었습니다.
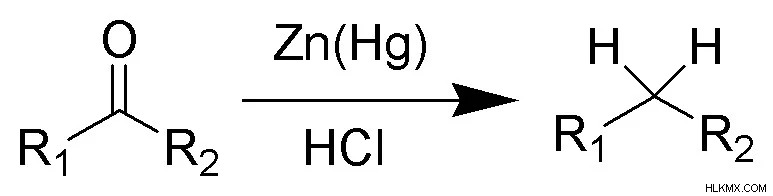
결론
탄화수소는 수소와 탄소의 두 원자로 구성된 유기 화합물입니다. 알킨은 적어도 하나의 탄소-탄소 삼중 결합을 함유하는 불포화 탄화수소이다. 알키네를 준비하는 몇 가지 방법이 있습니다. 이들 방법 중 일부는 알킬 디 하이드의 탈히 할로겐화, 칼슘 탄화물로부터의 알킨의 제조 및 디 하이알 리드로부터의 알키네 제제를 포함한다. 알키네스의 공식은 cnh2n-2입니다.