주요 차이 산성 및 염기성 아미노산 사이의 산성 아미노산은 중성 pH에서 산성 측쇄를 함유하는 반면, 기본 아미노산은 중성에서 염기성 측쇄를 함유한다는 것이다. pH . 또한, 산성 아미노산의 측쇄는 카르 복실 산기를 함유하는 반면, 염기 아미노산의 측쇄는 아미노기를 함유한다.
산성, 기본 및 중성 아미노산은 측쇄 또는 유기 R 그룹의 극성에 기초하여 특징 지어진 세 가지 유형의 아미노산입니다. 일반적으로, 아미노산은 아미노기 (-NH2), 카르 복실 그룹 (-COOH), 유기 R 기 및 중심 탄소 원자에 부착 된 수소 원자를 함유한다.
주요 영역을 다루었습니다
1. 산성 아미노산은 무엇입니까
- 정의, 사이드 체인, 중요성
2. 기본 아미노산이란 무엇입니까
- 정의, 사이드 체인, 중요성
3. 산성 및 기본 아미노산의 유사점은 무엇입니까
- 일반적인 기능의 개요
4. 산성 및 기본 아미노산의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어
산성 아미노산, 아미노기, 염기성 아미노산, 카르 복실 산기, 극성
산성 아미노산은 무엇입니까
산성 아미노산은 측쇄에 카르복실산 기 (-cooh)를 함유하는 극성 아미노산의 한 유형입니다. 그것은 의미합니다. 이들 아미노산은 아미노산 구조에 2 개의 카르복실산 기를 함유한다 :측쇄의 카르 복실 그룹은 하나의 카르 복실 그룹과 다른 하나는 중앙 탄소 원자에 부착된다. 따라서, 이것은 용액에서 PKA를 감소시킨다. 따라서, 산성 아미노산은 측쇄의 카르 복실 그룹에서 양성자를 잃을 수있어 산성 용액을 생성 할 수있다.
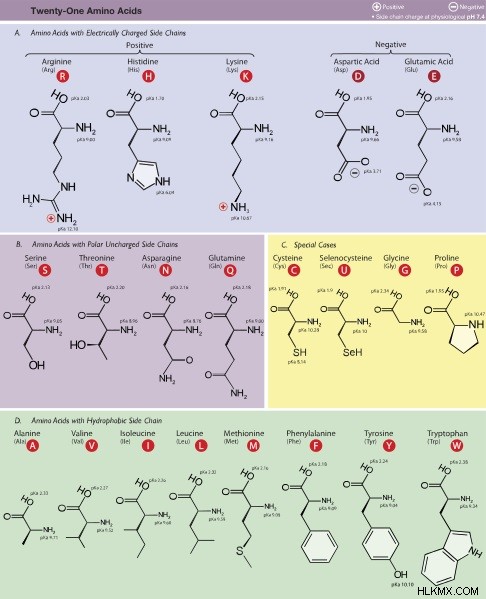
그림 1 :아미노산의 특성
두 가지 주요 유형의 산성 아미노산은 글루탐산과 아스파르트산입니다.
기본 아미노산
기본 아미노산은 다른 유형의 극성 아미노산입니다. 그것들은 측쇄에 아미노기 (-nh2)를 함유한다. 여기서도 기본 아미노산에는 2 개의 아미노산이 포함됩니다. 하나의 아미노기 그룹은 측쇄에서 발생하는 반면 두 번째 아미노기는 중심 탄소 원자에 부착됩니다. 산성 아미노산과는 반대로, 기본 아미노산은 높은 PKA로 구성됩니다. 따라서, 이는 측쇄에서 아미노기에 양성자를 얻어 기본 용액을 생성 할 수있게한다.
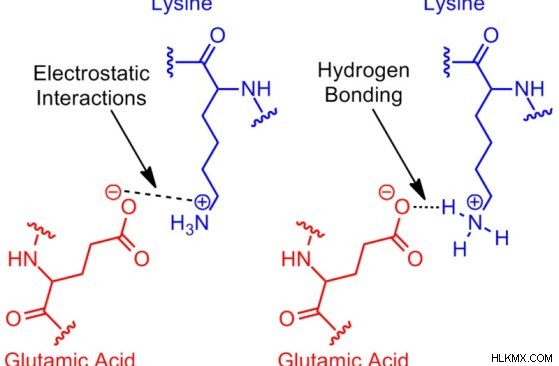
그림 2 :산성 및 기본 아미노산 간의 상호 작용
세 가지 유형의 기본 아미노산은 라이신, 아르기닌 및 오르 니틴입니다.
산성 및 염기 아미노산의 유사성
- 산성 및 염기성 아미노산은 유기 R 그룹의 특성에 기초하여 특징 지어진 두 가지 유형의 아미노산이다.
- 유기 R 그룹은이 아미노산에서 다른 극성으로 구성됩니다.
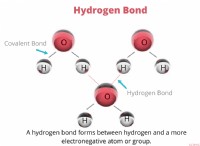
- 산성 아미노산과 기본 아미노산 사이의 수소 결합은 베타 시트를 형성하는 동안 중요합니다. 또한, 이들 아미노산은 단백질 서브 유닛을 결합하여 단백질의 3 차 구조를 형성한다.
- 또한, 두 유형의 아미노산은 촉매 부위로서 작용하여 생물학적 반응의 효소 촉매 작용 동안 다양한 대사 산물 및 산성 또는 염기성 중간체를 안정화시킨다. 또한, 이들은 2 차 결합 부위로서 작용함으로써 ATP의 가수 분해를 안정화시킨다.
산성 및 기본 아미노산의 차이
정의
산성 아미노산은 두 번째 산 부분을 갖는 아미노산을 지칭하고 염기성 아미노산은 두 번째 기본 그룹 (보통 아미노기)을 함유하는 아미노산을 나타냅니다.
측쇄/유기 R 그룹
산성 아미노산과 염기성 아미노산의 주요 차이점은 산성 아미노산은 중성 pH에서 산성 측쇄를 함유하고 기본 아미노산은 중성 pH에서 염기성 측쇄를 함유한다는 것입니다.
측쇄 구성 요소
산성 아미노산의 측쇄에는 카르 복실 산기 (-COOH)가 포함되어 있고 기본 아미노산의 측쇄에는 아미노기 (-NH2)가 포함됩니다. 따라서 이것은 산성 아미노산과 기본 아미노산의 또 다른 차이점입니다.
PKA
또한 산성 아미노산은 낮은 PKA 값으로 구성되며, 이는 양성자를 잃어 버릴 수있는 반면 기본 아미노산은 높은 PKA 값으로 구성되어 양성자 결합을 허용합니다.
충전
그들의 전하는 또한 산성 아미노산과 기본 아미노산의 차이입니다. 산성 아미노산은 측쇄에서 음전하를 지니고 기본 아미노산은 측쇄에서 양전하를 낳습니다.
예제
일부 산성 아미노산은 글루탐산과 아스파르트산이며, 세 가지 유형의 염기성 아미노산은 라이신, 아르기닌 및 오르니 틴입니다.
결론
산성 아미노산에는 측쇄에 카르 복실 그룹이 포함되어있어 음전하가 있습니다. 반면에, 기본 아미노산은 측쇄에 아미노기를 함유하여 양전하를 허용한다. 산성 및 염기성 아미노산 모두에 대한 이러한 전하는 단백질의 2 차 구조의 형성에 중요하다. 그것들은 생화학 적 반응의 효소 촉매 중에도 중요합니다. 따라서, 산성 아미노산과 염기성 아미노산의 주요 차이점은 측쇄에 존재하는 기능 그룹의 유형이다.
참조 :
1. Ophardt, Charles E.“아미노산의 특성과 특성.” vertual Chembook , 2003, 여기에서 구할 수 있습니다
이미지 제공 :
1. Dancojocari의“아미노산”-자체 WorkPrint it herethis w3c-unspecified 벡터 이미지는 Adobe Illustrator로 만들어졌습니다.이 SVG의 소스 코드는 유효합니다. (CC BY-SA 3.0) Commons Wikimedia
2를 통한. Commons Wikimedia를 통한 자체 작업 (공개 도메인)의“다음으로 Glutamic Acid Lysine Salt Bridge”를 다시 방문하십시오.