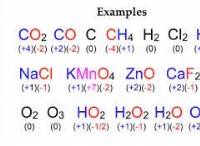
* 원자 반경은 다양합니다. 원자의 크기는 고정 값이 아닙니다. 그것은 다음을 포함한 몇 가지 요소에 따라 다릅니다.
* 요소 : 다른 원소마다 원자 반경이 다릅니다.
* 본딩 유형 : 금속에서, 원자는 금속 결합에 의해 함께 유지되며, 여기에는 금속 전자의 "바다"가 포함됩니다. 이것은 각 원자를 둘러싼 전자 구름이 크게 겹칠 수 있음을 의미합니다.
* 조정 번호 : 주어진 원자를 둘러싼 가장 가까운 이웃 원자의 수는 얼마나 밀접하게 포장 된 지에 영향을 미칩니다.
* 결정 구조 : 금속은 다양한 결정 구조 (예를 들어, 얼굴 중심 입방, 신체 중심 입방)에 존재하여 원자 사이의 거리에 영향을 미칩니다.
* 온도와 압력 : 이 요인들은 원자 사이의 간격에 영향을 줄 수 있습니다.
* 금속 결합 : 금속의 비편성 전자는 가단성, 연성 및 우수한 전도도에 기여합니다. 이들 전자는 개별 원자에 단단히 결합되지 않으므로 뚜렷한 원자 반경의 개념이 덜 명확하다.
단일 "크기"대신, 우리는 종종 다음과 같이 이야기합니다.
* 금속 반경 : 이것은 결정 격자에서 인접한 금속 원자 사이의 거리의 절반을 나타냅니다. 금속 구조에서 원자 사이의 간격을 설명하는 더 실용적인 방법입니다.
* 효과적인 이온 반경 : 어떤 경우에는 금속이 이온을 형성 할 수 있으며, 효과적인 이온 반경은 전하 및 조정 수에 따라 계산 될 수 있습니다.
특정 금속에서 원자 크기에 대한 구체적인 아이디어를 얻으려면 :
* 주기성 테이블을 참조하십시오 : 그것은 종종 다양한 요소에 대한 원자 반경을 나열합니다.
* 특정 금속에 대한 데이터를 찾으십시오 : 금속 반경 및 기타 관련 매개 변수에 대한 데이터를 제공하는 리소스가 있습니다.
요약하면, 금속에서 원자의 "크기"는 단순한 개념이 아닙니다. 다양한 요인에 의해 영향을 받고 금속 반경 또는 효과적인 이온 반경을 사용하여 설명 할 수있는 원자 간 간격에 대해 이야기하는 것이 더 적절합니다. .