이유는 다음과 같습니다.
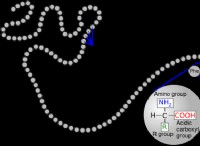
* 용해도는 분자 구조를 기반으로합니다. 물질의 용해도는 분자와 용매의 분자 사이의 인력에 의존한다.
* 물은 극지 : 물 분자는 (전자의 고르지 않은 공유로 인해) 양성 및 부정적인 목적을 가지므로 극성 용매가됩니다. 설탕이나 염과 같은 극성 분자는 물 분자와 강한 관광 명소를 형성 할 수 있기 때문에 물에 잘 녹아 들어갑니다.
* 지방은 비극성입니다 : 지방과 오일은 전자를 고르게 공유하는 긴 탄소 및 수소 원자 사슬로 구성됩니다. 이것은 그것들을 비극성으로 만들고, 물과 잘 섞이지 않습니다.
* "처럼 녹는 것처럼": 일반적인 규칙은 극성 물질이 극성 용매에 용해되고 비극성 물질이 비극성 용매에 용해된다는 것입니다.
예 :
* 오일과 물 : 오일은 비극성이며 물과 혼합되지 않습니다 (극성).
* 설탕과 물 : 설탕은 극성이며 물에 쉽게 용해됩니다.
예외 :
* 양서류 분자 : 일부 분자에는 극성 및 비극성 부품이 모두 있습니다. 이 분자들은 물과 지방 사이의 "교량"역할을 할 수있어 어느 정도 혼합 할 수 있습니다. 예로는 비누와 세제가 있습니다.
* 미셀 : 양친 매성 분자는 물에 미셀이라는 구조를 형성 할 수 있습니다. 분자의 비극성 꼬리는 함께 클러스터링되는 반면, 극세는 바깥쪽으로 향하고 물 분자와 상호 작용합니다. 이것은 지방과 기름을 물에 매달릴 수있게합니다.
요약 : 일부 물질은 물과 지방 모두에 적은 곳에 용해 될 수 있지만 동시에 두 가지 모두에 진정으로 용해 될 수는 없습니다.