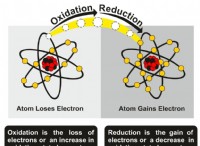
다음은 반응의 고장입니다.
* 반응 : 2NAOH (aq) + 2Al (S) + 6H₂O (L) → 2NA [Al (OH) ₄] (aq) + 3H₂ (g)
* 제품 :
* 나트륨 알루미 네이트 (Na [Al (OH) ₄]) 가용성 화합물이므로 용액에 용해됩니다.
* 수소 가스 (H₂) 가연성과 폭발성이므로 안전한 안전 위험이 있습니다.
이것이 문제인 이유 :
* 부식 : 반응은 알루미늄 용기가 부식되어 결국 실패하여 누출과 잠재적 오염을 유발합니다.
* 열 생성 : 발열 반응은 열을 생성하여 잠재적으로 용기가 과열되고 반응이 통제되지 않으면 폭발 할 수 있습니다.
* 수소 가스 생산 : 수소 가스의 형성은 위험한 가연성 대기를 만들어 화재 나 폭발의 위험을 증가시킵니다.
수산화 나트륨에 대한 대체 저장 옵션 :
* 폴리에틸렌 (PE) 용기 : 이들은 NAOH에 내성이 있으며 일반적으로 솔루션을 저장하고 운반하는 데 사용됩니다.
* 스테인레스 스틸 컨테이너 : 특정 등급의 스테인레스 스틸은 NAOH에 저항력이 있으며 저장에 사용될 수 있지만 올바른 등급을 사용하는 것이 중요합니다.
* 유리 용기 : 유리는 또한 NAOH를 저장하기에 적합한 재료이지만 파손을 피하기 위해주의 깊게 처리해야합니다.
결론 : 알루미늄 용기에 수산화 나트륨 용액을 저장하는 것은 부식성 반응, 열 생성 및 수소 가스 생산으로 인해 심각한 안전 위험을 초래할 수 있습니다. 화학 물질의 저장 및 취급에 항상 적절하고 호환되는 재료를 사용하십시오.