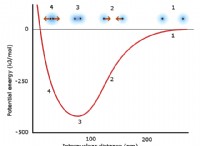
이 값은 상이한 온도에서의 반응 속도에 대한 실험 연구에서 얻어진다.
이 값이 관련된 이유는 다음과 같습니다.
* SN1 반응 : 테르-부틸 클로라이드의 가수 분해는 SN1 메커니즘 (치환 친 핵성 단 분자)을 통해 진행된다.
* 탄수화물 형성 : 이 반응에서의 속도 결정 단계는 고 에너지 중간체 인 테르-부틸 탄수화물의 형성이다.
* 활성화 에너지 : 활성화 에너지는 반응 분자가 전이 상태에 도달하고 반응을 진행하는 데 필요한 최소 에너지를 나타냅니다.
키 포인트 :
* 3 차 할로드 : 테르-부틸 클로라이드와 같은 3 차 할로드는 형성된 탄수화물의 안정성으로 인해 비교적 쉽게 SN1 반응을 겪습니다.
* 낮은 활성화 에너지 : 1 차 또는 2 차 할로드와 비교하여 테르-부틸 클로라이드의 가수 분해에 대한 낮은 활성화 에너지는 3 차 탄수화물의 안정성에 기인한다.
SN1 메커니즘 또는 활성화 에너지에 영향을 미치는 요인에 대한 자세한 정보를 원하시면 알려주십시오!