설명 :
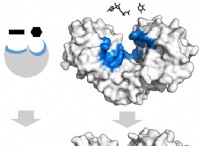
* 방향족 고리의 활성화 : 페놀의 하이드 록실기 (-oh)는 강하게 활성화 된 그룹이며, 이는 방향족 고리의 전자 밀도를 증가시킨다. 이로 인해 고리는 질산염과 같은 전자 성 공격에 더 취약합니다.
* 공명 안정화 : 페놀의 산소 원자에있는 전자 쌍의 전자 쌍은 방향족 고리로 비편화되어 공명 구조를 생성 할 수 있습니다. 이러한 공명 구조는 질화 동안 형성된 중간 탄수화물을 안정화시켜 반응을 더 유리하게 만듭니다.
질화 메커니즘 :
질화는 방향족 고리에서 니트로늄 이온 (NO2+)의 전자 성 공격을 포함한다. 페놀에서 하이드 록실기의 활성화 특성은 고리를보다 전자 풍부하게하여 전기성을보다 쉽게 끌어 들인다.
톨루엔과의 비교 :
톨루엔은 메틸 그룹 (-ch3)을 가지고 있으며,이 그룹은 약하게 활성화 된 그룹이다. 메틸기는 고리의 전자 밀도를 증가시키는 반면, 그 효과는 페놀에서 하이드 록실기의 효과보다 훨씬 덜 현저하다.
결론 :
하이드 록실 그룹의 강한 활성화 효과 및 공명 안정화로 인해, 페놀은 톨루엔보다 훨씬 빠르게 질화된다.