탄소 화합물 원소 탄소를 함유하는 화합물입니다. 수소를 제외한 다른 원소의 화합물보다 더 많은 탄소 화합물이 있습니다. 이들 중 대부분은 유기 화합물이지만 무기 탄소 화합물도 존재합니다. 다음은 탄소 화합물의 예, 그들이 함유 한 화학 결합의 유형 및 탄소 화합물이 분류되는 방법을 살펴 봅니다.
탄소 화합물의 예
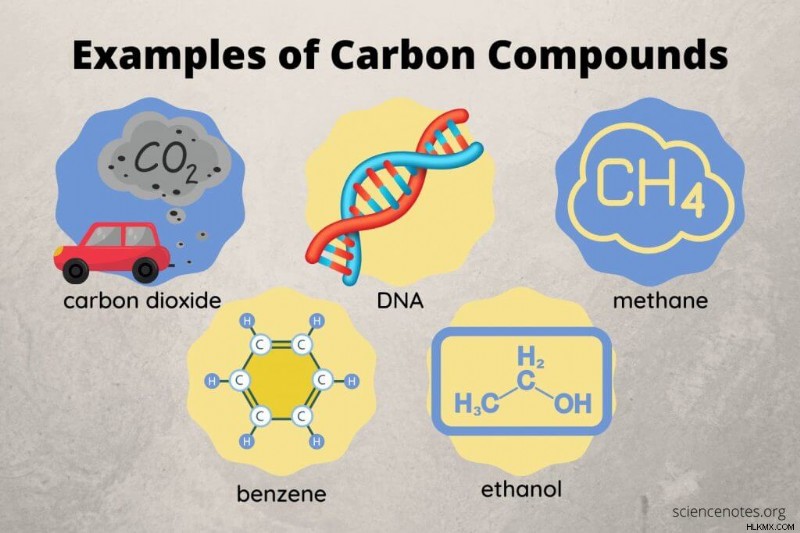
모든 유기 및 유기 금속 화합물 및 일부 무기 화합물은 탄소를 함유한다. 탄소 화합물의 예는 다음과 같습니다.
- 이산화탄소 (Co 2 )
- 데 옥시 리보 핵산 (DNA)
- 포도당 (c₆h₁₂o₆)
- 메탄 (ch 4 )
- 벤젠 (c 6 H 6 )
- 에탄올 (c₂h₆o)
- 시안화물 (HCN)
- 실리콘 카바이드 (sic)
- Phosgene (cocl 2 )
- 카본 산 (H 2 Co 3 )
- 탄소 테트라 플루오 라이드 (cf 4 )
- 아세트산 (ch₃cooh)
- 테트라 에틸 리드 [(ch₃ch₂) ₄pb]
탄소 화합물 분류
탄소 화합물은 유기, 유기 금속 또는 무기 일 수 있습니다.
- 유기 화합물 :유기 화합물은 항상 탄소와 수소를 함유합니다. 유기 화합물의 주요 부류에는 단백질, 지질, 탄수화물 및 핵산이 포함됩니다. 전통적으로 유기 화합물은 살아있는 유기체에서 발생하지만 실험실에서 합성 할 수도 있습니다.
- 유기 금속 화합물 :유기 금속 화합물은 적어도 하나의 탄소 금속 결합을 함유한다. 예를 들어 Ferrocene, Tetraethyl Lead 및 Zeise 's Salt. 가 있습니다
- 무기 탄소 화합물 :무기 화합물은 탄소를 함유하지만 수소는 아닙니다. 무기 화합물은 미네랄과 가스에서 발생합니다. 예는 일산화탄소 (CO), 이산화탄소 (Co <서브> 2 를 포함한다 ) 및 탄산 칼슘 (caco 3 ).
일부 화합물은 간단한 정의를 무시합니다. 예를 들어, 시안화물 (HCN)은 무기 화합물로 간주됩니다. 수소를 함유하고 일부 살아있는 유기체에 의해 생성되지만, 수소와 시안화물 그룹 사이의 결합은 공유보다 본질적으로 더 이온 성이다. 또 다른 예외는 Phosgene (cocl 2 입니다 )는 수소가 포함되어 있지 않지만 유기농은 포함되어 있습니다. Phosgene은 염소화 탄화수소 (유기 화합물)에서 나오고 탄소 원자의 화학적 결합의 특성으로 인해 유기적이기 때문입니다.
.탄소 동종
동종 요소는 순수한 요소의 다른 형태입니다. 여기서, 탄소 원자는 다른 탄소 원자와 결합한다. 동종 트로프는 무기 화합물입니다. 다음은 일부 탄소 할당량의 목록입니다.
- 다이아몬드
- 흑연
- 그래 핀
- 흑연
- diamane
- Fullerenes
- 비정질 탄소
- 탄소 나노 튜블
- 탄소 나노 폼
- 유리 탄소
- Lonsdaleite (육각형 탄소)
- 사이클로 카본
- 선형 아세틸렌 탄소
- 규정형 탄소
탄소 합금
여러 합금에는 탄소가 포함되어 있습니다. 탄소 합금에는 철강 및 주철이 포함됩니다. "순수한"금속조차도 코크스를 사용하여 제련되면 부분적으로 탄소 합금입니다. 예로는 아연, 알루미늄 및 크롬이 있습니다.
탄소 화합물의 화학 결합 유형
탄소는 일반적으로 그 자체 및 다른 유형의 원자와 공유 화학 결합을 형성합니다. 비극성 공유 결합은 다른 탄소 원자에 탄소 결합 될 때 형성됩니다. 극성 공유 결합은 비금속 또는 금속성에 탄소 결합 될 때 형성됩니다.
탄소는 금속에 결합 할 때 이온 결합을 형성합니다. 예를 들어, 탄소에서 탄소와 칼슘 사이의 화학적 결합 (CAC 2 )는 본질적으로 이온입니다.
그래 핀 내의 탄소-탄소 결합은 분비 된 전자를 포함하며 금속 결합입니다.
탄소 원자와 관련된 화학 결합 수
다른 원소를 갖는 결합 탄소 원자의 수는 산화 상태에 의존한다. 가장 일반적인 산화 상태는 +4 또는 -4 (사면체)이므로 탄소는 일반적으로 4 개의 결합을 형성합니다. 그러나 다른 탄소 산화 상태는 +3, +2, +1, 0, -1, -2 및 -3을 포함합니다. 몇몇 경우에, 탄소는 심지어 다른 원자와 6 개의 결합을 형성한다. 예를 들어, 헥사 메틸 벤젠 (c 12 h 18 ) 구조는 6 개의 다른 탄소 원자에 결합 된 단일 탄소 원자를 포함합니다!
탄소 화합물 명명
일부 유형의 탄소 화합물의 이름은 화학 성분을 나타냅니다.
- 탄화물 :탄화물은 전기 음성이 낮은 다른 원소를 갖는 탄소의 이진 화합물이다. al 4 c 3 , cac 2 , SIC, TIC 및 WC는 탄화물의 예입니다.
- Carboranes :카보 란은 탄소와 붕소의 분자 클러스터이며, 종종 수소가 있습니다. Carborane의 예는 H 2 입니다 c 2 b 10 H 10 .
- 탄소 할라이드 :탄소 할라이드는 탄소와 할로겐을 함유한다. 탄소 할라이드의 예는 탄소 테트라 요오드 라이드 (CI <서브> 4 를 포함한다 ) 및 탄소 테트라 클로라이드 (CCL <서브> 4 ).
탄소 화합물의 특성
탄소 화합물은 다양한 화학 물질 그룹을 포함하지만 공통 특성을 공유합니다.
- 탄소의 주요 특성은 촉진 또는 체인과 고리를 형성하는 능력입니다. 따라서 많은 탄소 화합물에는 고리 또는 긴 사슬 또는 형태 중합체가 포함됩니다.
- 대부분의 탄소 화합물은 실온에서 반응성이 낮지 만 가열 될 때 활발하게 반응합니다. 예를 들어, 연료는 가열 될 때까지 안정적입니다.
- 많은 탄소 화합물은 가연성입니다.
- 많은 탄소 화합물은 비극성입니다. 비극성이기 때문에 종종 물에 용해도가 낮습니다. 그렇기 때문에 물만 기름이나 그리스를 자르지 않습니다.
- 질소가있는 탄소의 화합물은 종종 폭발적입니다. 원자 사이의 결합은 불안정하고 깨질 때 상당한 에너지를 방출합니다.
- 탄소와 질소의 화합물은 종종 액체와 같은 뚜렷하고 불쾌한 냄새를 갖는다. 일반적으로 고형물은 무취입니다.
탄소 화합물의 사용
이름을 지정할 수있는 모든 응용 프로그램은 탄소 화합물을 사용합니다. 모든 살아있는 유기체에는 탄소가 포함되어 있습니다. 연료와 식품은 탄소 기반입니다. 플라스틱, 안료, 살충제 및 많은 합금은 탄소 화합물입니다.
참조
- 면, F. Albert; Murillo, Carlos A., Bochmann, Manfred (1999). 고급 무기 화학 (6th ed.). Wiley-Interscience. ISBN 978-0471199571.
- Dresselhaus, M.S.; Dresselhaus, G.; Avouris, Ph., eds. (2001). "탄소 나노 튜브 :합성, 구조, 특성 및 응용". 응용 물리학의 주제 . 80. 베를린. ISBN 978-3-540-41086-7.
- 해리스, P.J.F. (2004). “상업용 유리 카본의 풀러렌 관련 구조”. 철학 잡지 . 84 (29) :3159–3167. doi :10.1080/14786430410001720363
- Ritter, Stephen K. (2016). “탄소에 대한 6 개의 채권 :확인됨”. 화학. 잉그 뉴스 . 94 (49) :13. doi :10.1021/cen-09449-scicon007
- Simpson, P. (1993) 유기 화학 :프로그래밍 된 학습 접근법 . 뛰는 것. ISBN 978-0412558306.