나트륨 원자 (NA)
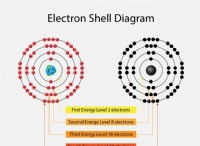
* 전자 구성 : 1S² 2S² 2P⁶ 3S¹
* 원자가 전자 : 1 (3S 궤도의 고독한 전자)
나트륨 이온 (Na+)
* 전자 구성 : 1S² 2S² 2p⁶
* 원자가 전자 : 0
변화
나트륨 원자가 나트륨 이온 (Na+)이되면 단일 원자가 전자 를 잃습니다. . 이 전자는 이온 결합을 형성하기 위해 다른 원자, 일반적으로 비금속에 기증된다. 이 전자의 손실은 나트륨 이온에 전체 외부 쉘 (2p 쉘)을 남겨두고 더 안정적으로 만듭니다.
키 포인트
* 안정성 : 이온은 전자의 외부 껍질을 갖기 때문에 상응하는 중성 원자보다 더 안정적입니다.
* 충전 : 전자를 잃는 것은 전자보다 더 많은 양성자가 있기 때문에 나트륨 이온에 양전하 (+1)를 제공합니다.
* 옥트 규칙 : 나트륨은 전자를 잃어 버림으로써 고귀한 가스 네온 (NE)과 같은 안정적인 전자 구성을 달성하여 옥트 규칙을 충족시킵니다.