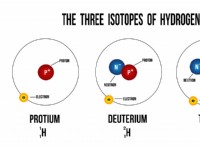
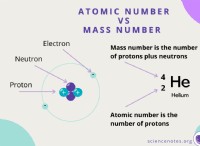
1. 전자 구조 :
* 에너지 수준 : 원자 및 분자의 전자는 특정 에너지 수준에서 존재합니다. 화합물이 에너지 (열이나 빛과 같은)를 흡수하면 전자는 더 높은 에너지 수준으로 점프 할 수 있습니다.
* 여기 상태 : 여기 상태는 불안정하고 전자는 원래 에너지 수준으로 빠르게 떨어집니다.
* 방출 : 전자가 뒤로 떨어지면 흡수 된 에너지를 빛으로 방출합니다. 이 방출 된 빛의 색상은 여기 상태와 접지 상태의 에너지 차이에 따라 다릅니다.
2. 색상과 에너지 :
* 가시 스펙트럼 : 가시 광선 스펙트럼은 바이올렛 (가장 높은 에너지)에서 빨간색 (가장 낮은 에너지)에 이릅니다.
* 특정 에너지 전환 : 화합물은 다른 전자 구조를 가지므로 에너지 수준 간격이 다릅니다. 이것은 여기와 지상 상태의 에너지 차이가 각 화합물에 대해 독특하다는 것을 의미합니다.
* 색 방출 : 방출 된 빛은 에너지 차이에 해당합니다. 에너지 차이가 작은 화합물은 적혈구를 방출하는 반면 에너지 차이가 커지는 화합물은 바이올렛 라이트를 방출합니다.
3. 기타 요인 :
* 분자 구조 : 분자 내에서 원자와 결합의 배열은 전자 구조와 에너지 수준에 영향을 미칩니다.
* 화학 환경 : 용매 또는 온도와 같은 주변 환경은 또한 에너지 수준과 방출 된 빛의 색상에 영향을 줄 수 있습니다.
요약 : 화합물의 가시 방출의 색상은 빛에 의해 여기 될 때 전자가 겪는 특정 에너지 전이에 의해 결정됩니다. 이러한 전이는 분자 구조와 화학 환경에 의해 영향을받는 화합물의 독특한 전자 구조에 의해 결정됩니다.
예 :
* 화염 테스트에서 나트륨 (NA) : 나트륨 원자는 화염에서 에너지를 흡수하여 전자가 더 높은 에너지 수준으로 점프하게됩니다. 그들은 지상 상태로 돌아 오면서 나트륨의 특징 인 황색 빛을 방출합니다.
이것은 단순화 된 설명이며 형광 및 인광과 같은 더 복잡한 측면이 있습니다. 그러나이 설명은 왜 다른 화합물이 다른 색상의 빛을 방출하는지에 대한 기본적인 이해를 제공합니다.