1. 구성 요소 이해 :
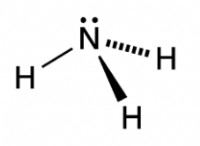
* 황 (s) : 황산의 중앙 원자.
* 수소 (H) : 이름의 산 부분은 수소의 존재를 의미합니다.
* 산소 (O) : "황제"의 "IC"접미사는 더 높은 산화 상태에서 산소의 존재를 나타냅니다.
2. 요소 결합 :
* 수소 : 산은 전형적으로 용액에서 양성자 (H+)로 방출 될 수있는 하나 이상의 수소 원자를 갖는다.
* 황 : 황은 황산에서 일반적인 산화 상태 +6을 갖는다.
* 산소 : 산소는 일반적으로 산화 상태가 -2입니다.
3. 균형 산화 상태 :
* 중성 화합물을 달성하려면 산화 상태의 합은 0과 같아야합니다.
* 우리는 황의 +6 산화 상태의 균형을 맞추려면 두 개의 수소 원자 (각각 +1)가 필요합니다.
* 산소의 -2 산화 상태의 균형을 맞추려면 4 개의 산소 원자가 필요합니다.
4. 공식 :
모든 것을 종합하면 황산의 화학적 공식은 h₂so₄ 입니다. .