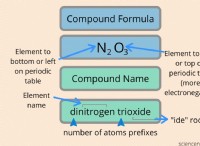
1. 이온을 식별하십시오 :
* 철 두 가지 공통 이온을 형성 할 수 있습니다.
* fe² fe (철 이온)
* fe³ fe (이온)
* 설페이트 포뮬러 so₄²⁻ 를 갖는 다 원자 이온이다 .
2. 요금 결정 :
* 철 이온 (Fe²⁺)은 +2 전하가 있습니다.
* 제제 이온 (Fe³⁺)은 +3 전하가 있습니다.
* 황산염 이온 (So₄²⁻)은 -2 전하를 갖습니다.
3. 요금의 균형 :
철 황산기의 경우 * :
* 요금의 균형을 맞추려면 하나의 fe²⁺ 이온과 하나의 so₄²⁻ 이온이 필요합니다.
* 이것은 우리에게 공식 feso₄ 를 제공합니다 .
황산 제 2 철의 경우 :
* 요금의 균형을 맞추려면 2 개의 fe³⁺ 이온과 3 개의 So₄²⁻ 이온이 필요합니다.
* 이것은 우리에게 공식을 제공합니다 .
따라서 철 황산염의 화학적 공식은 철의 산화 상태에 따라 다릅니다.
* 철 황산염 : FESO₄
* 황산 제 2 철 : fe₂ (so₃) ₄