금속 문자
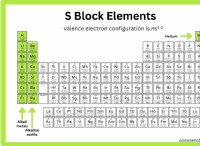
* 정의 : 금속 특성은 요소가 양의 이온 (양이온)을 형성하기 위해 전자를 어떻게 쉽게 잃는지를 나타냅니다. 이 속성은 일반적으로 주기성 테이블의 아래로 이동하고 왼쪽으로 증가합니다.
* 주요 요인 :
* 전기 음성 : 전기 음성이 낮은 요소는 전자를 잃을 가능성이 높습니다 (더 많은 금속성).
* 이온화 에너지 : 이온화 에너지가 낮은 요소 (전자를 제거하기 쉬운)는 금속성입니다.
* 원자 크기 : 더 큰 원자는 핵으로부터 외부 전자를 추가하여 제거하기가 더 쉬워집니다 (금속성).
세 번째 기간
주기율표의 3 번째 기간에는 나트륨 (NA)에서 아르곤 (AR)까지의 요소가 포함됩니다. 왼쪽에서 오른쪽으로 기간을 가로 질러 이동하면 금속 문자가 감소합니다.
3 번째 기간에 따른 요소
다음의 요소 * 다음 * 3 번째 기간은 4 번째 기간에있을 것입니다. 이러한 요소는 다음과 같습니다.
* 칼륨 (k)
* 칼슘 (ca)
* Scandium (SC)
* 티타늄 (ti)
* 바나듐 (V)
* 크롬 (CR)
* 망간 (Mn)
* 철 (Fe)
* 코발트 (CO)
* 니켈 (NI)
* 구리 (Cu)
* 아연 (Zn)
* 갈륨 (GA)
* 게르마늄 (GE)
* 비소 (AS)
* 셀레늄 (SE)
* 브롬 (Br)
* 크립톤 (KR)
답변
이 요소들 중 칼륨 (k) 가장 금속성 특성을 가질 것입니다. 이유는 다음과 같습니다.
* 위치 : 그것은 강한 금속 특성으로 유명한 첫 번째 열 (알칼리 금속)에 있습니다.
* 전기 음성 : 전기 음성이 매우 낮습니다.
* 이온화 에너지 : 이온화 에너지가 상대적으로 낮습니다.
중요한 참고 : 4 번째 기간 (스칸듐 및 티타늄과 같은)의 원소는 금속이지만, 주기율 테이블의 위치로 인해 칼륨이 가장 금속성이 될 것입니다.