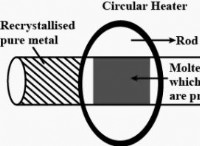
다음은 고장입니다.
* 산 분리 : 산 (HA)이 물에 용해 될 때, 물 분자에 양성자 (H+)를 기증하여 히드로 늄 이온 (H3O+) 및 산의 컨쥬 게이트 염기 (A-)를 형성 할 수있다.
* ha + h2o h h3o + + a-
* 평형 상수 (KA) : 이 반응의 평형 상수를 산 해리 상수 (KA)라고합니다. 평형에서 반응물에 대한 생성물의 비율을 나타냅니다.
* ka =[h3o+] [a-] / [ha]
더 높은 KA 값은 더 강한 산 :를 나타냅니다 이는 산이 양성자를 기증 할 가능성이 높아서 더 높은 농도의 H3O+ 이온 및 더 낮은 농도의 해독되지 않은 산 (HA)을 의미한다.
자세한 내용이나 예제를 원하시면 알려주세요!