이온 전하 이해
* 원자 물질의 기본 빌딩 블록이며 중립 전하 (동일한 수의 양성자 및 전자)가 있습니다.
* 이온 전자를 얻거나 잃어버린 원자로 순 양성 또는 음전하가 발생합니다.
* 양이온 전자를 잃어 버려 형성된 양으로 하전 된 이온입니다.
* 음이온 전자를 얻음으로써 형성된 음으로 하전 된 이온이다.
이온 전하 계산
1. 요소를 식별하십시오 : 작업중 인 요소 (예 :나트륨, 염소)를 결정하십시오.
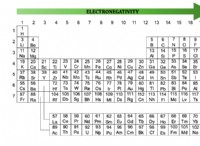
2. 원자 번호를 찾으십시오 : 원자 수는 원자의 핵에서 양성자 수입니다. 주기적인 테이블에서 찾을 수 있습니다.
3. 원자가 전자 수를 결정하십시오 : 원자가 전자는 원자의 가장 바깥 에너지 수준의 전자입니다. 주기율표의 그룹 번호 (열)를 사용하여 도움을 줄 수 있습니다.
* 그룹 1, 2 및 13-18 (헬륨 제외)은 그룹 번호와 동일한 수의 원자가 전자를 갖습니다.
* 전이 금속 (그룹 3-12)은 더 복잡하며 전자 구성에 대한 더 깊은 이해가 필요합니다.
4. 이온 전하 예측 :
* 금속 (주기율표의 왼쪽)은 양이온을 형성하기 위해 전자를 잃는 경향이 있습니다. 이들은 일반적으로 그룹 수와 동일한 이온 전하를 형성합니다 (예를 들어, 그룹 1의 나트륨 (NA)은 1 전자가 Na ⁺가되기 위해 1을 잃습니다).
* 비금속 (주기성 테이블의 오른쪽)은 음이온을 형성하기 위해 전자를 얻는 경향이 있습니다. 그들은 일반적으로 그룹 수 (예 :그룹 17의 염소 (CL)가 CL이되기 위해 1 전자를 얻는 것)와 같은 8 마이형 이온 전하를 형성합니다.
5. 이온 전하를 쓰십시오 : 양이온을 사용하여 전하를 나타내고 양이온에 대한 플러스 (+) 표시를 배치하고 음이온의 마이너스 (-) 표시를 표시합니다.
예
마그네슘 (mg)의 이온 전하를 계산합시다.
1. 요소 : 마그네슘 (Mg)
2. 원자 번호 : 12
3. 원자가 전자 : 마그네슘은 그룹 2에 있으므로 2 개의 원자가 전자가 있습니다.
4. 이온 전하 : 마그네슘은 2 개의 원자가 전자를 잃어 +2 전하의 양이온이 될 것입니다.
5. 이온 전하 : mg²⁺
중요한 메모
* 이온 전하 예측은 일반적인 규칙이며 예외가 있습니다. 일부 요소는 다른 전하로 여러 이온을 형성 할 수 있습니다.
* 전이 금속은 여러 이온을 형성 할 수 있습니다. 전이 금속 이온에 대한 특정 전하를 알기 위해 표 또는 컨텍스트를 참조해야 할 수도 있습니다.
다른 예를 통해 작업하고 싶다면 알려주세요!