핵심 개념
이 기사에서는“타우토머 화”의 의미, 에놀 안정성의 경향, 산성 및 기본 조건 하에서 중요한 메커니즘을 포함하여 케토 에놀 타우토머 화에 대해 배웁니다.
Keto Enol Tautomerization이란 무엇입니까?
케토 에놀 타우토머 화는 케톤의 구조와 에놀 분자 사이의 전환의 반응이다. 우리가 그러한 반응의 메커니즘을 거치기 전에 먼저“토이체 화”의 의미를 명확히합시다.
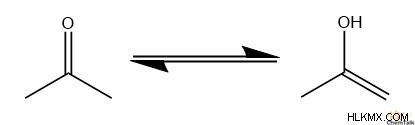
화학자들은“타우토머 화”라는 용어를 사용하여 동적 평형 상태 하에서 상호 연결되는 두 분자 구조의 과정을 설명합니다. 종종 이것은 분자의 두 부위 사이의 일부 화학 그룹의 움직임을 포함합니다.
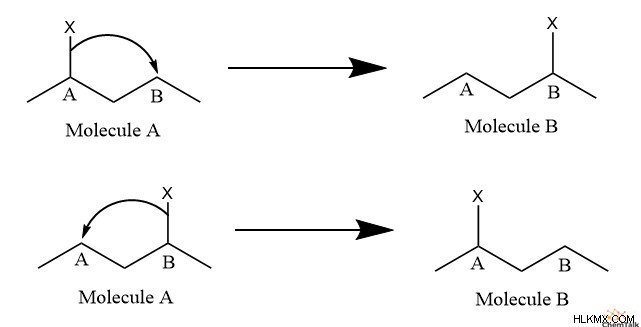
다르게 말하면, 일부 기능성 그룹 X가있는 분자 A가 있다고 가정 해 봅시다. 분자 A에서 그룹 X는 사이트 A에 부착됩니다. 그러나 그룹 X가 부착 된 또 다른 적절한 위치가 있습니다. 부위 B라고 불리는 그룹 X가 부위 A에서 사이트 B로 이동하여 분자 A를 분자 B로 변경합니다. 사이트 B에 도달하면 그룹 X는 사이트 A로 다시 이동할 수 있습니다. 분자 구조를 변환하는 사이트 간 그룹 X의 움직임을 타우토머 화라고합니다.
.
용매에 용해 된 두더지와 같은 분자 A의 전체 무리가있는 경우, 분자 B로 지속적으로 전환되고 다시 되돌아갑니다. 그러나, 분자 A 및 분자 B의 상대적 비율은 일관성을 유지한다. 결국 전환율이 상쇄되기 때문이다. 이것이 화학자들이“동적 평형”의 의미입니다.
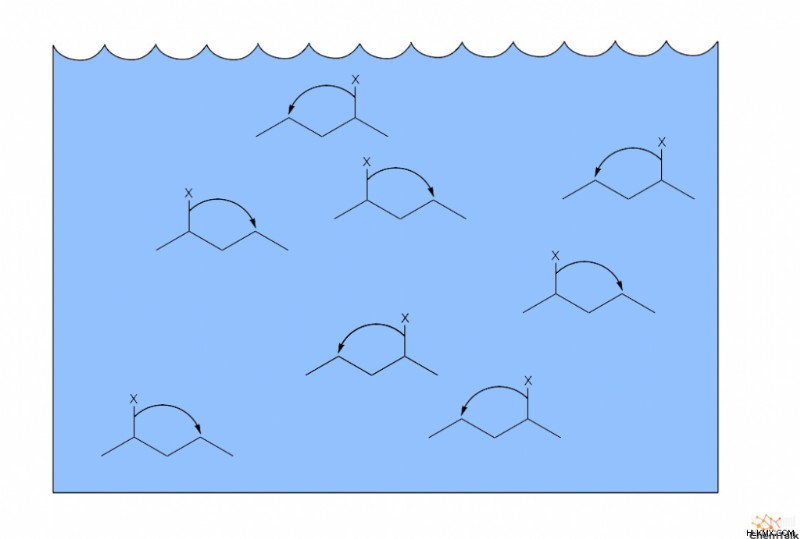
종종, 분자 A는 분자 B보다 안정성이 더 높습니다. 이 불평등 한 평형 상태는 케톤과 에놀을 포함하여 팽팽한 쌍에서 일반적으로 발생합니다. 그러나 Keto Enol tautomerization에서 상이한 구조적 인자가 다른 분자보다 다른 분자를 초과하는 것을 결정합니다.
케토 Enol Tautomer 구조
일반적으로, 케톤은 가장 흔한 분자 구조에서 에놀보다 크게 선호된다. 그러나, ɑ- 탄소의 구조 (카르 보닐에서 한 번에 압도 된 탄소)는 케톤의 호의를 바꿀 수 있습니다.
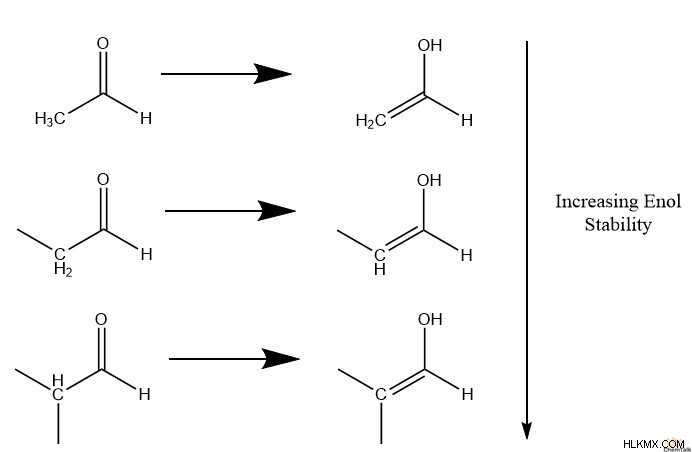
그러한 구조적 경향 중 하나는 더 많은 비 이수성이있는 ɑ-charbons가 Enol과 같은 안정성을 더 많이 가지고 있다고 주장합니다. 예를 들어, ɑ- 탄소에 메틸 구조가 있고 3 개의 하이드로겐이있는 경우, 2 개의 수소가있는 메틸렌 ɑ- 탄소보다 에놀을 형성하는 안정성이 적습니다. 메틸렌에 의해 형성된 에놀은 하나의 수소와 2 개의 탄화수소 부착물을 갖는 메틴 ɑ-carbons보다 적은 에놀을 안정화시킵니다.
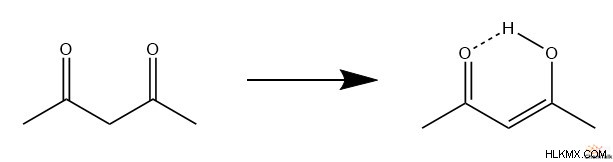
그러나, 에놀 형태가 케톤보다 우세한 일부 분자가 존재한다. 그러한 예 중 하나는 1,3- 디 카보 닐 분자이며, 이는 종종 특정 ALDOL 응축으로부터 형성됩니다. 이 분자에서, 에놀은 형성되어 산화물 이온에 수소를 섞을 수 있습니다. 이 새로운 수산화물 구조는 인접한 카보 닐로부터 안정화되어 수소 결합을 제공한다. 궁극적으로,이 에놀-케톤 조합은 6 원 링의 특성을 갖는이 자기 안정화 구조를 형성합니다.
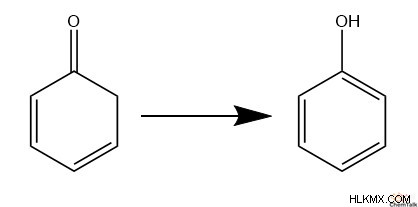
방향족 에놀은 또한 안정성을 갖는 경향이 있으며, 방향족은 케톤보다 안정성을 제공하기 때문이다. 구체적으로, 생성 된 알켄이 방향족 전자 사이클을 완료 할 때 에놀이 선호된다. 이것은 페놀이 안정적인 구조를 형성하는 경향이있는 이유를 설명하는 반면 2,4- 사이클로 디엔은 드물게 남아있는 경향이 있습니다.
케토 enol 동성상 화 메커니즘
산성 조건 하에서 타우토머 화
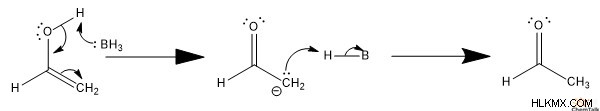
산성 조건 하에서 케토 에놀 호변 이성질체는 본질적으로 케톤과 에놀 사이의 전환을 주도하는 양성자 화를 가지고있다.
에놀을 형성하기 위해, 산은 카르 보닐 상에 고독한 전자 쌍을 양성한다. 그런 다음, 산의 활용체는 ɑ- 탄소를 반란으로 옮깁니다. 이것은 전자를 전달하여 궁극적으로 Enol을 형성합니다.
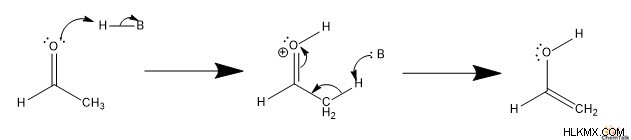
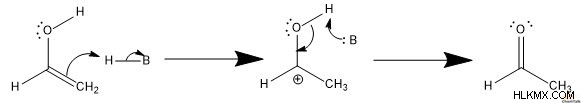
케톤을 형성하기 위해, 산은 알켄을 양성하여 ɑ- 탄소와 양성자 사이에 C-H 결합을 형성한다. 이어서, 컨쥬 게이트 염기는 수산화물을 탈 로토 팅한다. 산화물 음이온으로부터의 고독한 쌍은 탄수화물과 PI 결합을 형성하여 케톤을 초래한다.
.
기본 조건 하에서 타우토머 화
기본 조건 하에서 케토 에놀 호변 이성질체는 본질적으로 de 을 갖는다 -케톤과 에놀 사이의 전환을 주도하는 프로토 톤.
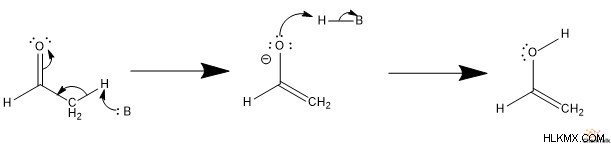
Enol을 형성하기 위해 일반적인 Brønsted-lowry base는 ɑ-carbon을 멸균합니다. 이것은 카르 보닐의 PI 전자를 구동하여 탈 양성자 화 된 탄소와 알켄 PI 결합을 형성한다. 그런 다음, 컨쥬 게이트 산은 산화물 음이온을 양성하여 enol을 형성합니다.
.
케톤을 형성하기 위해, 염기는 수산화물을 탈퇴하여 고독한 전자 쌍을 방출한다. 그런 다음이 전자는 카르 보닐을 형성하여 고독한 전자 쌍을 ɑ- 탄소로 밀어 넣습니다. 그런 다음, 컨쥬 게이트 산은 ɑ- 탄소를 양성하여 케톤을 형성합니다
.