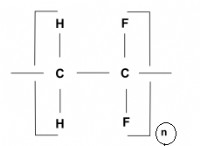
* 전자 구성 : 붕소는 [HE] 2S² 2P¹의 전자 구성을 가지고 있으며 실리콘은 [NE] 3S² 3P²를 가지고 있습니다. 둘 다 3 개의 원자가 전자를 가지지 만, 주요 양자 수의 차이 (붕소의 경우 2, 실리콘의 경우 3 개)는 원자 크기와 전기 음성의 상당한 차이를 초래합니다.
* 원자 크기 : 실리콘은 붕소보다 상당히 큽니다. 이 더 큰 크기는 결합 길이, 결합 강도 및 반응성에 영향을 미칩니다.
* 전기 음성 : 실리콘은 붕소보다 전기 음성이 적습니다. 이는 실리콘이 결합으로 전자를 유치 할 가능성이 적어 결합 거동과 화학적 반응성에 영향을 미친다는 것을 의미합니다.
* 산화 상태 : 붕소는 일반적으로 +3 산화 상태에서 화합물을 형성하는 반면, 실리콘은 일부 화합물에서 +2, +4 및 -4의 산화 상태에 존재할 수있다.
* 결합 행동 : 붕소는 주로 공유 결합을 형성하며, 종종 전자 결핍 화합물을 형성합니다. 실리콘은 공유 결합 및 이온 결합을 모두 형성 할 수있다.
* hydrides : 붕소는 디보 레인 (B₂H₆)과 같은 복잡한 수 소화물을 형성하며, 이는 비정상적인 결합을 나타냅니다. 실리콘은 실란 (sih₄)과 같은 간단한 수평물을 형성합니다.
화학적 특성의 몇 가지 주요 차이점은 다음과 같습니다.
* 산화물의 산도 : 산화 붕소 (b (o₃)는 산성이고, 이산화 실리콘 (Sio₂)은 양서류입니다 (산 또는 염기로서 작용할 수 있음).
* 물과의 반응성 : 붕소는 물에 상대적으로 반응하지 않는 반면 실리콘은 온수와 반응하여 실리콘을 형성합니다.
* 할리 드의 형성 : 붕소는 붕소 트리 플루오 라이드 (BF₃)와 같은 트리 할리드를 형성하는 반면, 실리콘은 실리콘 테트라 클로라이드 (SICL)와 같은 테트라 할리드를 형성합니다.
요약 :
붕소와 실리콘은 주기율표에서 동일한 그룹을 공유하지만, 원자 크기, 전기 음성 및 전자 구성의 차이로 인해 화학적 특성이 크게 다릅니다.