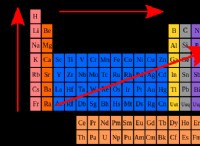
1. 원자 번호 : 주기율표의 기본 기준은 원자 번호이며, 이는 원자의 핵의 양성자 수를 나타냅니다. 요소는 원자 번호의 순서가 높아집니다.
2. 전자 구성 : 원자의 에너지 수준에서 전자의 배열은 화학적 거동을 결정합니다. 동일한 그룹 (수직 컬럼)의 요소는 가장 바깥 쪽 쉘 (밸런스 쉘)에 유사한 전자 구성을 가지므로 유사한 화학적 특성을 초래합니다.
3. 주기적 트렌드 : 요소의 특성에서 예측 가능한 패턴입니다.
* 전기 음성 : 화학적 결합으로 전자를 유치하는 원자의 경향. 전기 음성은 일반적으로 기간에 걸쳐 증가하고 그룹을 감소시킵니다.
* 이온화 에너지 : 원자에서 전자를 제거하는 데 필요한 에너지. 이온화 에너지는 일반적으로 기간에 걸쳐 증가하고 그룹을 감소시킵니다.
* 전자 친화력 : 전자가 중성 원자에 첨가 될 때 에너지의 변화. 전자 친화력은 일반적으로 기간에 걸쳐 증가하고 그룹을 감소시킵니다.
* 원자 반경 : 핵에서 가장 바깥 쪽 전자 쉘까지의 거리. 원자 반경은 일반적으로 기간에 걸쳐 감소하고 그룹을 낮추게됩니다.
* 금속 문자 : 요소가 전자를 잃고 양성 이온 (양이온)을 형성하는 경향. 금속성 특성은 일반적으로 그룹을 증가시키고 기간에 걸쳐 감소합니다.
4. 그룹 및 기간 :
* 그룹 (수직 열) : 그룹 내의 요소는 동일한 수의 원자가 전자를 가지기 때문에 유사한 화학적 특성을 공유합니다.
* 기간 (수평 행) : 기간 내의 요소는 동일한 수의 전자 쉘을 갖습니다.
5. 블록으로의 분류 :
* s- 블록 : 그룹 1 및 2 (알칼리 금속 및 알칼리성 지구 금속)의 요소, S 궤도에 가장 바깥 쪽 전자가 있습니다.
* p- 블록 : 그룹 13-18의 요소, p 궤도에 가장 바깥 쪽 전자가있는 요소.
* d- 블록 : 그룹 3-12의 금속 전이, d 궤도에서 가장 바깥 쪽 전자.
* f- 블록 : F 궤도에 가장 바깥 쪽 전자가있는 란타나이드 및 액티 나이드.
6. 화학 행동 예측 :
이러한 추세를 이해함으로써 화학자들은 다음을 수행 할 수 있습니다.
* 요소의 반응성을 예측합니다 : 불소와 같은 전기 음성 요소는 반응성이 높고, 칼륨과 같은 전기 음성 요소는 더 반응성이 높습니다.
* 화학 결합의 형성을 이해하십시오 : 유사한 전기성이있는 요소는 공유 결합을 형성하는 반면, 큰 차이가있는 것은 이온 결합을 형성합니다.
* 요소를 다른 클래스로 분류합니다. 금속, 비금속, 금속성 등
주기율표 법은 요소의 행동을 이해하고 예측하기위한 강력한 프레임 워크를 제공합니다. 특성을 기반으로 요소를 구성하고 분류하는 능력은 화학자에게 없어서는 안될 도구가됩니다.