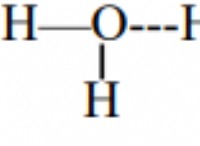이유는 다음과 같습니다.
* 에탄은 비극성 분자입니다. 탄소 하이드로겐 결합으로 에탄의 대칭 구조는 모든 쌍극자 모멘트를 취소하여 분자를 비극성으로 만듭니다.
* 런던 분산 세력은 가장 약한 유형의 분자간 힘입니다. 그것들은 분자 주변의 전자 분포의 일시적인 변동으로 인해 일시적인 쌍극자를 만듭니다. 그런 다음이 임시 쌍극자는 인접 분자에서 쌍극자를 유도하여 약한 관광 명소를 초래할 수 있습니다.
쌍극자 쌍극자 상호 작용 및 수소 결합은 더 강한 힘이지만 극성 분자에서만 발생합니다. 에탄은 비극성이기 때문에,이 힘은 존재하지 않습니다.