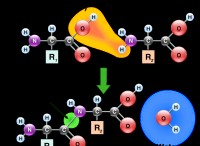
* 분자 형상 : Xenon Pentafluoride는 정사각형 피라미드 분자 형상을 가지고 있습니다. 이것은 5 개의 불소 원자가 중앙 크세논 원자 주위에 배열되어 정사각형 피라미드를 형성 함을 의미합니다. 크세논 원자의 고독한 전자 쌍은 피라미드의 정점에 위치합니다.
* 전기 음성 차이 : 불소는 크세논보다 훨씬 더 전기 음성입니다. 이는 불소 원자가 전자 밀도를 그들 자신으로 끌어 당겨 불소 원자에 부분 음전 전하 (Δ-)를 생성하고 크세논 원자에 부분 양전하 (Δ+)를 생성한다는 것을 의미한다.
* 비대칭 : 사각형 피라미드 형상은 비대칭 적입니다. Xenon 원자의 전자 쌍과 불소 원자의 배열은 이온 내에서 전자 밀도의 고르지 않은 분포를 생성한다.
* 쌍극자 모멘트 : 고르지 않은 전하 분포와 비대칭 기하학으로 인해, Xenon Pentafluoride 이온은 영구 쌍극자 모멘트를 가지므로 극성 분자가됩니다.