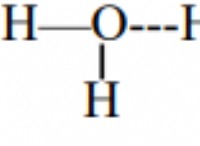* 강산 : 강한 산은 용액에서 완전히 이온화 (이온으로 분리)하는 것입니다. 이는 모든 분자가 물에 양성자 (H+)를 기증하여 하이드로 늄 이온 (H3O+)을 형성 함을 의미합니다. 예 :염산 (HCL), 황산 (H2SO4), 질산 (HNO3).
* 희석 용액 : 희석 용액은 용매 (보통 물)에 비해 상대적으로 낮은 농도의 용질 (용해 된 물질)을 갖는다.
합치기 :
* 강산 분자의 낮은 농도가 있으면 강산이 희석 될 수 있습니다 솔루션에서.
* 존재하는 산 분자는 완전히 이온화 될 것이지만, 이들 중 단순히 시작하는 것만으로도, 전체적으로 H3O+ 이온의 농도가 낮아지고 산성 용액이 적습니다.
예 :
* 큰 물 용기에 농축 황산 (매우 강함) 한 방울을 상상해보십시오. 황산 방울은 완전히 이온화되지만 물의 양에 비해 너무 작기 때문에 H3O+ 이온의 전체 농도가 낮아서 용액이 희석됩니다.
키 포인트 :
*희석은 *강도 *가 아니라 산의 *농도 *에 영향을 미칩니다. 강산은 농도에 관계없이 항상 완전히 이온화됩니다. 그러나, 강산의 희석 용액은 동일한 산의 농축 용액보다 덜 산성 일 것이다.