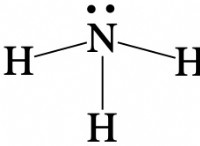
분자 기하학의 분해는 다음과 같습니다.
* 탄소의 본딩 : 펜탄의 각 탄소 원자는 다른 탄소 또는 수소 원자와 4 개의 단일 결합을 형성합니다. 이것은 사면체 형상 를 따릅니다 여기서, 4 개의 결합이 탄소 원자 주위에 사면체 형태로 약 109.5 °의 결합 각도가 배열된다.
* 전체 모양 : 사슬의 각 탄소는 사면체 형상을 가지기 때문에 전체 펜탄 분자는 엄격하게 선형이 아닙니다. zigzag 모양 가 있습니다 결합 각으로 인해.
중요한 참고 : 펜탄 (N- 펜탄, 이소 펜탄 및 네오펜탄)의 세 가지 이성질체가 있으며, 각각은 탄소 사슬의 약간 다른 배열을 갖는다. 그러나, 각 탄소 원자 주변의 기본 기하학은 사면체로 남아있다.