주요 차이-반응물 대 제품
반응물과 제품은 화학 반응의 두 가지 주요 구성 요소입니다. 반응물은 화학 반응의 시작 재료입니다. 제품은 반응이 완료된 후 발견 될 수있는 화학 종이다. 산-염기 반응, 산화 환원 반응 및 연소 반응과 같은 다양한 유형의 화학 반응이 있습니다. 따라서 동일한 반응물은 때때로 관련된 반응 유형에 따라 다른 생성물을 제공합니다. 주요 차이 반응물과 생성물 사이에는 반응물이 반응 전체에 걸쳐 소비되는 반면 생성물은 반응으로 형성된다는 것입니다.
주요 영역을 다루었습니다
1. 반응물이란 무엇입니까
- 정의, 특성, 반응 유형 및 반응물
2. 제품이란 무엇입니까
- 정의, 속성, 반응 유형 및 제품
3. 반응물과 제품의 유사점은 무엇입니까
- 일반적인 기능의 개요
4. 반응물과 제품의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어 :산-염기 반응, 연소 반응, 분해 반응, 흡열 반응, 발열 반응, 침전 반응, 생성물, 반응물, 산화 환원 반응, 합성 반응
반응물이란 무엇입니까
반응물은 화학 반응의 출발 물질로 작용하는 화학 종입니다. 반응물은 화학 반응의 진행 동안 소비됩니다. 반응의 끝에서, 반응물 중 어느 것도 반응 혼합물에 존재할 수 없지만, 때로는 일부 반응물이 끝에 존재할 수있다.
.반응물은 무색이거나 화려 할 수 있습니다. 반응의 유형과 조건에 따라 결국 무색이거나 화려한 제품을 초래할 수 있습니다. 화학 반응의 반응물은 고체 상, 액체 상 또는 기체상 일 수있다. 반응의 유형에 따라 반응물은 다양합니다.
반응 및 반응물의 유형
산-염기 반응
이 반응의 반응물은 산과 염기입니다.
산화 환원 반응
반응물은 산화제와 감소 제입니다. 때로는 완충액 용액도 반응 혼합물의 pH를 유지하는 데 사용됩니다.
합성 반응
합성 반응의 반응물은 제품보다 작은 분자입니다.
분해 반응
분해 반응에서 반응물은 그 반응의 생성물보다 큰 분자입니다.
연소 반응
연소 반응의 반응물은 가연성 화학 종입니다.
강수 반응
대부분의 경우, 침전 반응의 반응물은 액체입니다.
발열 반응
이러한 화학 반응의 반응물은 제품보다 잠재적 에너지가 더 높습니다.
흡열 반응
이러한 반응의 반응물은 제품보다 잠재적 인 에너지가 낮습니다.
반응 속도는 반응물에 의해 영향을받습니다. 특정 반응의 속도는 반응물의 잠재적 에너지에 달려 있습니다.
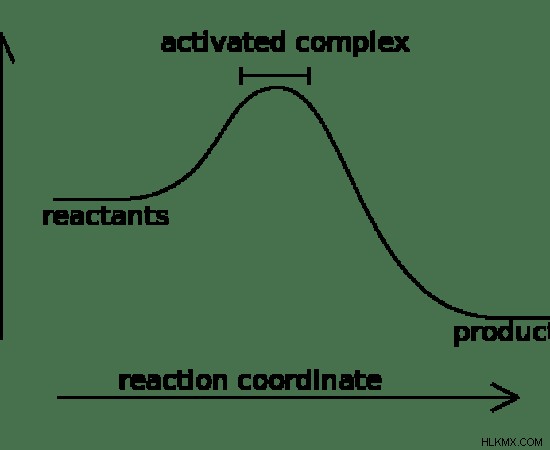
그림 01 :발열 화학 반응에 대한 반응 좌표 다이어그램
위의 이미지는 특정 화학 반응에 대한 반응 좌표 다이어그램을 보여줍니다. 이 반응에서, 반응물은 생성물보다 높은 잠재적 에너지를 갖는다. 따라서이 반응의 진행 중에 과도한 에너지가 주변에 방출됩니다.
제품이란 무엇입니까
제품은 화학 반응의 결과로 형성된 물질입니다. 이 제품은 이온 또는 분자 일 수 있습니다. 특정 화학 반응의 생성물은 고체 상, 액체 상 또는 기체상에서 발생할 수 있습니다.
제품은 무색이거나 화려 할 수 있습니다. 제품의 색상은 반응에 관여하는 반응물의 유형에 따라 다릅니다. 반응 혼합물에 존재하는 생성물의 양은 항상 반응의 진행에 따라 증가합니다.
반응의 유형 및 제품
산-염기 반응
이 반응의 산물은 항상 소금과 물입니다.
산화 환원 반응
생성물은 산화되고 환원 된 형태의 반응물이있다. 종종 물은 제품으로 주어집니다.
합성 반응
합성 반응의 생성물은 반응물보다 큰 분자입니다.
분해 반응
분해 반응에서 제품은 반응물보다 작은 분자입니다.
연소 반응
연소 반응의 생성물은 종종 이산화탄소 및 물로 (탄화수소의) 완전한 연소 및 불완전한 연소를위한 일산화탄소입니다.
강수 반응
침전 반응의 생성물은 고체 침전물 또는 현탁액입니다.
발열 반응
이러한 화학 반응의 산물은 반응물보다 잠재적 에너지가 낮습니다.
흡열 반응
이러한 반응의 산물은 반응물보다 높은 잠재적 에너지입니다.
반응 속도는 특정 기간에 형성된 제품의 양에 의해 결정될 수 있습니다. 대부분의 경우 제품은 안정적인 형태의 반응물입니다. 반응물은 안정적인 상태를 얻기 위해 화학 반응을 겪습니다.
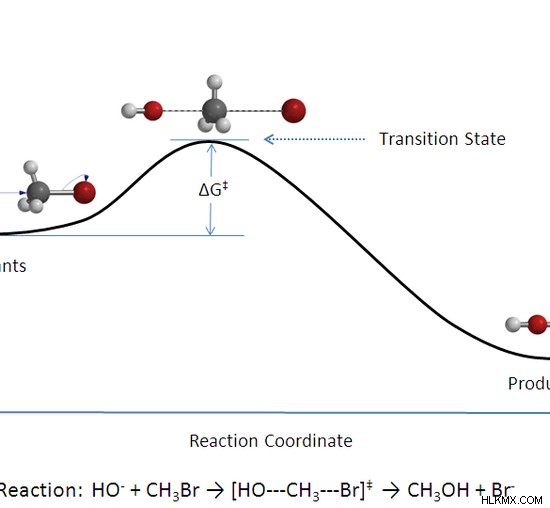
그림 02 :메틸 알코올 형성을위한 반응 조정 다이어그램
위의 다이어그램에서 반응 혼합물은 처음에 반응물만으로 구성되며 나중에 반응물의 전이 상태 인 중간 생성물이 있으며 최종 생성물이 형성됩니다. 반응물은이 특정 반응에서 생성물보다 더 높은 잠재적 에너지를 가지기 때문에 에너지는 열로 방출됩니다. 그러나이 에너지는 물질이 아니기 때문에 화학 반응의 산물로 간주되지 않습니다.
반응물과 생성물의 유사성
- 반응물과 생성물은 원자, 이온 또는 분자 일 수 있습니다.
- 반응물과 생성물 모두 반응 혼합물에 존재합니다.
- 반응물 및 제품은 화학 반응 속도를 결정하는 데 사용될 수 있습니다.
반응물과 제품의 차이
정의
반응물 : 반응물은 화학 반응의 출발 물질로 작용하는 화학 종입니다.
제품 : 제품은 화학 반응의 결과로 형성된 물질입니다.
소비
반응물 : 반응물은 반응 내내 소비됩니다.
제품 : 제품은 반응에서 소비되지 않습니다.
농도
반응물 : 반응 혼합물에 존재하는 반응물의 양은 반응 동안 빠르게 또는 천천히 감소합니다.
제품 : 반응 혼합물에 존재하는 생성물의 양은 반응 동안 빠르게 또는 천천히 증가합니다.
시작
반응물 : 반응의 시작시 반응 혼합물에 반응물 만 존재합니다.
제품 : 반응의 시작시, 제품은 반응 혼합물에 존재하지 않습니다.
종료
반응물 : 반응이 끝나면 반응물이 반응 혼합물에 존재하거나 존재하지 않을 수 있습니다.
제품 : 반응의 끝에, 생성물은 반응 혼합물에 존재한다.
결론
반응물과 제품은 화학 반응의 필수 구성 요소입니다. 반응물은 서로 반응하여 주요 제품 및 부산물을 만듭니다. 그러나 반응물은 화학량 론에 따라 반응합니다. 때때로 특정 반응물의 양은 다른 반응물과 완전히 반응하기에 충분하지 않을 수 있습니다. 이 경우, 생성물과 과량의 반응물 중 일부는 반응의 끝에 존재할 것이다. 그러나 여기서, 나머지 반응물은 반응의 결과로 형성되지 않기 때문에 반응의 산물로 간주되지 않는다. 따라서 반응물과 제품의 차이를 이해하는 것이 매우 중요합니다.
참조 :
1. Helmenstine, Ph.D. 앤 마리. “화학의 제품은 무엇입니까? 정의와 예.” 사고. N.P., N.D. 편물. 여기에서 사용할 수 있습니다. 2017 년 7 월 13 일.
2. libretexts. "화학 반응 속도." 화학 libretexts. LibreTexts, 2016 년 7 월 21 일. 웹. 여기에서 사용할 수 있습니다. 2017 년 7 월 13 일.
이미지 제공 :
1. 사용자에 의한“AC Com”:Slashme-en :이미지 :AC_COM.PNG (Public Domain)를 통해 wikimedia
2. Commons Wikimedia를 통해 자신의 작업 (CC By-SA 3.0)의“RXN 좌표 다이어그램 5”-Wikimedia