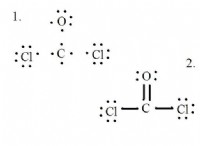산화 감소 이해 (산화 환원) 반응
* 산화 : 전자 손실
* 감소 : 전자의 이득
이온의 형성
* 이온은 원자가 전자를 얻거나 잃을 때 형성됩니다.
함께 모으는
산화 환원 반응에서 이온을 형성하려면, 하나는 전자를 쉽게 잃어 버릴 수있는 한 쌍의 물질이 필요하며, 다른 하나는 전자를 쉽게 얻는다 (감소).
예제 쌍
1. 나트륨 (NA) 및 염소 (CL)
* 나트륨 (NA)은 양의 이온 (Na+)을 형성하기 위해 하나의 전자를 잃는 경향이 있습니다.
* 염소 (CL)는 음성 이온 (Cl-)을 형성하기 위해 하나의 전자를 얻는 경향이 있습니다.
* 반응 : 2 Na + Cl2 → 2 NaCl
2. 마그네슘 (mg) 및 산소 (O)
* 마그네슘 (mg)은 양의 이온 (mg2+)을 형성하기 위해 2 개의 전자를 잃습니다.
* 산소 (O)는 2 개의 전자를 얻기 위해 음의 이온 (O2-)을 형성합니다.
* 반응 : 2 mg + O2 → 2 mgo
3. 아연 (Zn) 및 구리 (Cu)
* 아연 (Zn)은 구리보다 전자를 잃을 가능성이 높습니다.
* 반응 : Zn + Cu2 + → Zn2 + + Cu
키 포인트
* 더 많은 반응성 요소 (활동 시리즈에서 더 높음)는 산화되는 것 (전자를 잃는 것)이 될 것입니다.
* 반응성이 적은 요소는 감소하는 요소가 될 것입니다 (전자 게인).
* 결과 이온은 이온 결합을 통해 화합물을 형성합니다.
더 많은 예를 원하거나 활동 시리즈를 더 자세히 탐색하고 싶다면 알려주십시오!