Cocl2 (Phosgene Gas)와 같은 분자의 공식 전하를 결정할 때는 각 원자에 대한 원자가 전자의 수와 분자의 루이스 구조를 알아야합니다.
밸런스 전자 번호
주기적인 요소 테이블에서 각 원자를 찾아 원자가 전자의 수를 결정하십시오.
두 개의 전자가 첫 번째 S 쉘에 들어가고, 두 번째 S 쉘에 2 개의 전자, 첫 번째 P 쉘의 6 개의 전자 등을 상기시켜줍니다.
요금을 조정하십시오. 분자가 이온 인 경우 최종 전하를 설명하기 위해 하나 이상의 전자를 전반적으로 첨가하거나 빼냅니다.
Cocl2 (Phosgene Gas)의 경우 :C =4; o =6; Cl =7. 분자는 이온화되지 않았으며 중립 전하를 갖는다. 따라서 원자가 전자의 총량은 4 + 6 + (7x2) =24입니다.
Lewis Structure
Cocl2 (Phosgene Gas)의 Lewis 구조에 대한 다이어그램을 참조하십시오. 루이스 구조는 분자의 가장 안정적이고 가능한 구조를 나타냅니다. 원자는 쌍을 이루는 원자가 전자로 그려집니다. 옥트 규칙을 만족시키기 위해 고독한 전자 사이에 채권이 형성됩니다.
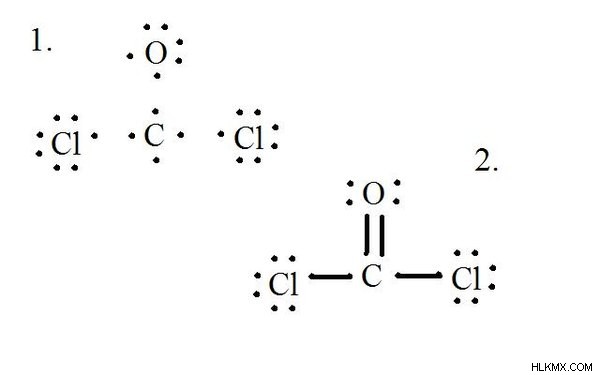
각 원자와 원자가 전자를 그린 다음 필요에 따라 결합을 형성합니다.
염화물 원자는 탄소 분자와 단일 결합을 공유하는 반면, 산소 원자는 탄소와 이중 결합을 형성합니다. 최종 구조의 각 원자는 옥트 규칙을 충족시키고 8 개의 원자가 전자를 갖는 분자 안정성을 허용합니다.
각 원자의 공식 전하
-
전이 금속을 함유하는 분자에 대한 공식 전하를 계산하는 것은 까다로울 수 있습니다. 전이 금속의 원자가 전자의 수는 고귀한 가스 같은 코어 외부의 수가 될 것입니다.
루이스 구조에서 각 원자의 고독한 쌍을 세십시오. 각 원자가 하나의 전자를 참여하는 각 결합에서 할당하십시오. 이 숫자를 함께 추가하십시오. Cocl2 :C =0 고독한 쌍과 결합 =4 개의 전자에서 4 개의 전자. O =1 쌍에서 4 개의 전자와 결합에서 2 개의 전자 =6 전자. CL =6 개의 전자 쌍으로부터의 전자는 C =7 전자와 결합에서 1 개의 전자를 + 1 전자.
비 결합 원자의 원자가 전자 수에서 합계를 빼십시오. 결과는 해당 원자에 대한 공식적인 전하입니다. Cocl2 :C =4 원자가 전자 (v.e.)에서 루이스 구조 (L.S.) =0 공식 전하 O =6 V.E. -6 L.S. =0 공식 전하 Cl =7 V.E. -7 L.S. =0 형식 전하
루이스 구조의 원자 옆에 이러한 전하를 씁니다. 전체 분자에 전하가있는 경우 오른쪽 상단의 괄호 안에 쓴 전하와 함께 Lewis 구조를 괄호로 둘러싸십시오.