이유는 다음과 같습니다.
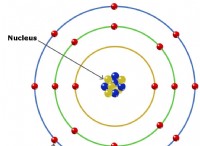
* 전자 구성 원자의 상이한 에너지 수준과 하천 내에서 전자의 배열을 설명한다. 이 배열은 양자 역학의 원리에 의해 지배되며, 이는 특정 공간 영역에서 전자를 찾을 확률을 정의합니다.
* 궤도 전자가 발견 될 가능성이 가장 높은 핵 주변의 영역을 나타냅니다. 각 궤도는 최대 2 개의 전자를 유지할 수 있으며 전자가 차지하는 특정 궤도는 원자의 전자 구성을 결정합니다.
* 본딩 원자 사이에서 전자가 공유되거나 전달 될 때 발생하여 분자 내의 전자 분포에 더 영향을 미칩니다.
따라서 원자 또는 분자의 전자 구성을 이해하면 전자가 발견 될 가능성이있는 위치를 예측할 수 있습니다.