이유는 다음과 같습니다.
* 금속 안정적인 전자 구성을 달성하기 위해 전자를 잃는 경향이 있습니다.
* 비금속 안정적인 전자 구성을 달성하기 위해 전자를 얻는 경향이 있습니다.
* 이온 결합 금속 원자가 전자를 비금속 원자로 전달할 때 형성되어 서로를 끌어들이는 반대로 하전 된 이온을 만듭니다.
예를 들어, 알루미늄 (AL)은 산소 (O)와의 이온 결합을 형성하여 산화 알루미늄 (Allool)을 생성합니다. 알루미늄은 3 개의 전자를 잃어 +3 이온 (Al³⁺)이되기 위해 3 개의 전자를 잃고, 산소는 2 개의 전자를 얻기 위해 -2 이온 (O²⁻)이됩니다. 이 반대로 하전 된 이온들 사이의 매력은 화합물을 함께 유지한다.
다른 용어를 명확히하겠습니다.
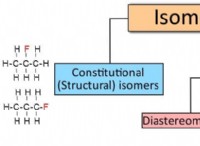
* 공유 결합 두 비금속 원자 사이에 전자 공유를 포함합니다.
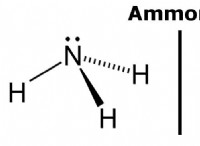
* 다 원자 이온 황산염 (SO₄²⁻) 또는 암모늄 (NH₄⁺)과 같은 순 전하가있는 원자 그룹입니다.
알루미늄 자체는 다 원자 형태로 존재하지 않습니다. 금속 특성을 가진 단일 요소입니다.