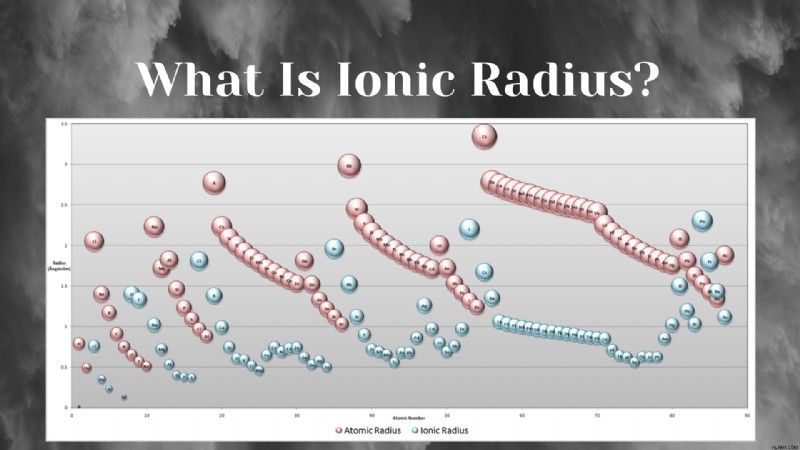
이온 반경 원자는 원자가 결정 격자 내에있을 때 원자의 이온을 측정 한 것입니다. 이온 반경은 간신히 만지는 두 개의 다른 원자 사이의 거리의 절반으로 정의됩니다.
이온 반경 추세 요소의 이온 반경이 요소의주기적인 표에서 예측 가능한 경향을 따르는 방법을 나타냅니다. 이온 반경은 주기적 테이블 아래로 위에서 아래로 이동함에 따라 증가하는 경향이 있으며 주기율표를 가로 질러 왼쪽으로 오른쪽으로 움직일 때 감소하는 경향이 있습니다.
이온 반경 정의
언급 한 바와 같이, 이온의 이온 반경은 원자가 결정 격자에있을 때 측정된다. 이온 반경의 값은 서로 거의 닿지 않는 두 이온 사이의 절반의 거리입니다. 전자 껍질의 경계는 정확한 판독 값을 얻기가 어렵 기 때문에 원자의 이온은 일반적으로 단단한 구인 것처럼 처리됩니다. 이온 반경은 원자 반경보다 약간 작거나 클 수 있습니다.
그것이 더 크든 작은 지 여부는 이온이 가지고있는 전하의 종류에 따라 다릅니다. 양이온, 또는 양으로 하전 된 이온은 일반적으로 요소의 중성 원자보다 작습니다. 이는 양이온이 쉘에서 전자가 제거 되었기 때문에 남아있는 전자는 핵에 더 큰 인력을 경험하고 그쪽으로 끌어 당기기 때문입니다. 대조적으로, 음이온 (음으로 하전 된 이온)은 추가 전자를 갖는다. 이 전자는 전자 구름의 전체 크기를 증가시키고 이온 반경을 더 크게 만들 수 있습니다.
이온 크기를 결정하는 데 사용되는 방법에 따라 변동 할 수 있기 때문에 이온 반경을 정확하게 측정하기가 어렵습니다. 이온 반경은 종종 X- 선 결정학 또는 유사한 장치 및 시스템으로 측정되며 다른 측정 시스템을 구현하면 이온 반경의 측정 값을 변경할 수 있습니다. 즉, 이온 반경의 대부분의 측정은 오후 30시에서 200시 사이입니다.
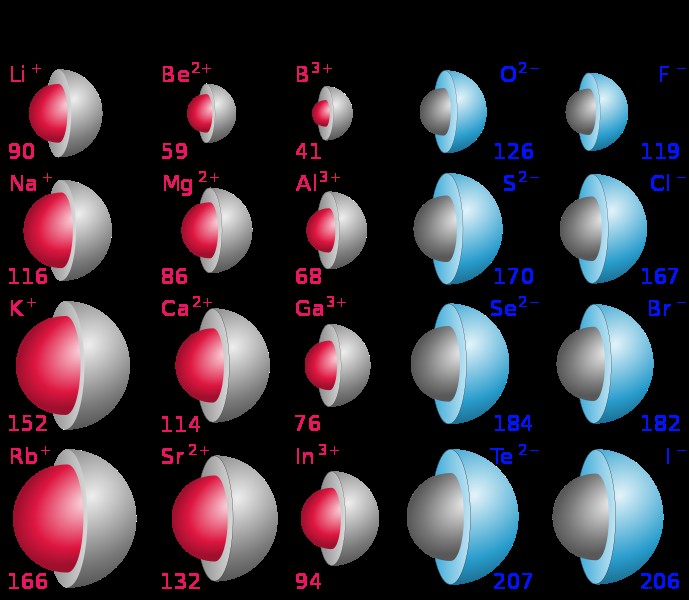
이온 반경과 원자 반경은 고정 된 값이 아닙니다. 이온과 원자의 다양한 구성이 이온의 핵 사이의 거리에 영향을 줄 수 있기 때문에 변화 될 수 있습니다. 두 개의 다른 원자의 전자 껍질은 서로 겹칠 수 있으며, 다른 상황은 겹치는 거리에서 이동할 수 있습니다.
.간신히 만지지 않는 두 원자의 원자 반경은 때때로 반 데르 발스 반경이라고도합니다. 이것은 반 데르 발스 (Van der Waals)의 주가 매력이 두 개의 다른 원자의 거리에 영향을 미치는 방식 때문입니다. 고귀한 가스 요소는 Van der Waals 반경으로 자주보고됩니다. 격자 내부의 금속의 공유 결합은 원자 반경이 금속 반경 또는 공유 반경이라고도 할 수 있음을 의미합니다. 때로는 비금속 요소 사이의 거리는 공유 반경이라고도합니다.
차트에 종종 주어진 원자 반경은 종종 반 데르 발스 반경, 공유 반경 및 금속 반경 값의 혼합물입니다. 이 값에는 작은 차이만이 있으며 대부분의 경우 차이는 아무런 문제가 아닙니다.
이온 반경 경향
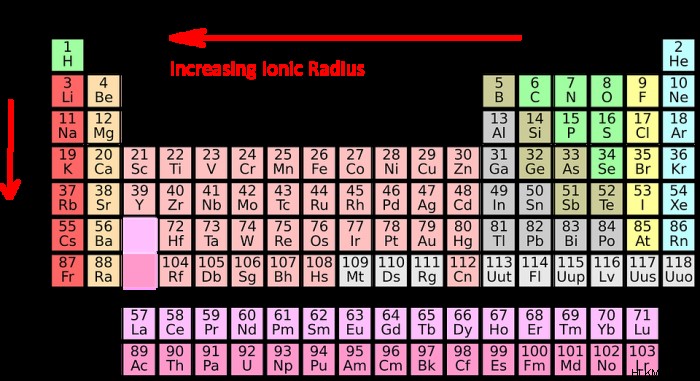
이온 반경 추세는 주기율표를 가로 질러 움직일 때 이온 반경이 따르는 예측 가능한 패턴을 설명합니다. 주기적인 테이블을 위에서 아래로 아래로 따라 요소 그룹 (컬럼)을 따라 다음 요소의 이온 반경이 증가합니다. 이는 주기율표 아래에 요소가 더 많은 전자 쉘을 가지므로 원자의 기본 크기를 증가시키기 때문에 발생합니다. 모든 주요 에너지 수준에는 작은 에너지 수준에서 발견되는 궤도보다 큰 궤도가 있습니다. 원칙 에너지 수준의 증가는 원자의 핵 전하 증가보다 높아서 원자 반경이 증가합니다.
특정 요소 기간 (또는 행)에서 주기율표를 왼쪽으로 따라 가면 요소의 이온 반경이 감소 함을 알게됩니다. 원자 핵의 크기가 더 큰 원자 숫자로 증가하기 때문에 처음에는 반 직관적 인 것처럼 보일 수 있습니다. 그러나 이것은 원자 핵의 크기가 증가함에 따라 원자의 전자에 영향을 미치는 양의 힘의 양도 증가하기 때문에 발생합니다. 이것은 핵의 크기가 증가함에 따라 원자의 전자가 더 단단히 그려진다는 것을 의미합니다. 원자 내의 전자는 원자의 양전하가 증가하여 원자의 핵에 점차 더 가까이 당겨집니다. 이 추세에는 몇 가지 예외가 있습니다. 예를 들어, 산소 반경은 실제로 질소의 반경보다 약간 큽니다.
이 효과는 양이온을 형성하기 때문에 금속 요소에서 매우 주목할 만하다. 원자는 가장 바깥 쪽 전자를 흘리며 때로는 전체 전자 쉘이 원자에서 떨어집니다. 그럼에도 불구하고, 주어진 기간 내의 전이 금속의 이온 반경은 시리즈의 시작 근처에서 원자에서 원자까지 크게 변동하지 않습니다.
.이온 반경 경향의 예
이온 반경 추세의 몇 가지 예를 살펴 보겠습니다. 주기율표의 그룹 1의 요소를 살펴 보겠습니다.
- 리튬 :원자 반경 - 1.34
나트륨 :원자 반경 - 1.54
칼륨 :원자 반경 - 1.96
Rubidium :원자 반경 - 2.11
세슘 :원자 반경 - 2.25
이제주기 테이블의 그룹 17 내의 일부 요소를 살펴 보겠습니다.
- 불소 :원자 반경 - 0.72
염소 :원자 반경 - 0.99
브롬 :원자 반경 - 1.14
요오드 :원자 반경 - 1.33
주기율표의 다른 트렌드
원자 반경 추세는 위에서 아래로 주기성 테이블을 따라 가면 발생하는 원자 반경의 변화를 반영합니다. 이온 반경과 마찬가지로 주기성 테이블을 아래로 이동함에 따라 다른 요소의 원자 반경은 증가하는 경향이 있습니다. 전기 음성 트렌드는 왼쪽에서 오른쪽으로 오른쪽으로주기적인 테이블을 따라 가면서 위에서 아래로 이동할 때 추세에서 아래쪽으로 증가하는 동안 어떻게 증가하는 경향이 있습니다.
.전자 친화도 경향은 주기성 테이블을 가로 질러 왼쪽에서 오른쪽으로 이동함에 따라 요소의 전자 친화력이 어떻게 증가하는지, 테이블 상단에서 하단으로 이동할 때 일반적으로 어떻게 감소되는지를 나타냅니다. 이온화 에너지 추세는주기적인 테이블을 사용하여 원자에서 전자를 대체하는 데 필요한 에너지의 양이 어떻게 추적 될 수 있는지를 나타냅니다. 주기적인 테이블을 위에서 아래로 따라 가면 이온화 에너지가 일반적으로 왼쪽으로 오른쪽으로 이동하면 증가하는 동안 증가합니다.







