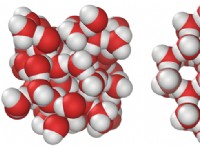
물은 알코올보다 전기를 더 잘 수행하여 단락을 유발합니다. 또한 물은 금속을 부식시키는 반면 알코올은 그렇지 않습니다. 물은 알코올보다 증발하는 데 시간이 오래 걸립니다.
전화가 미끄러 져서 컵에 빠졌을 때 지적 자극을 위해 차 한 잔으로 스마트 폰에서 Scienceabc 기사를 즐기고 있었을 때 한 번 기억하십니까?
기존의 지혜는 액체와 전자 장치가 함께 가지 않지만 차가 당신의 휴대 전화에 정확히 무엇을했는지 알고 있습니까? 또한 알코올이 차를 대체했다면 결과가 동일했을 것입니까?
답은 물과 알코올의 화학적 및 물리적 특성의 차이로 설명됩니다.
물 화학
물 분자는 화학적 공식 H2O로 표시되는 하나의 산소 원자에 결합 된 2 개의 수소 원자를 갖는다. 산소와 수소는 전자 쌍을 공유함으로써 결합을 형성하며, 쌍의 각 전자는 각각 수소와 산소에 의해 기증된다. 이것을 공유 결합이라고합니다. 전자 공유의 결과는 전기를 전도 할 자유 전자가 없다는 것입니다. 실제로, 순수한 탈 이온수는 전기를 전도하지 않습니다.
산소는 수소보다 더 많은 전자를 끌어들이는 놀라운 특성을 가지고 있습니다 ( 전기 음성 ). 물 분자에서, 전자 쌍은 산소와 수소에 더 단단히 결합된다. 따라서, 부분 음전하는 O 원자에서 발생하고 부분 양전하는 H 원자에서 발생한다. 물 분자의 기하학은 전하가 분리되어 있도록 (양의 중심과 음전하가 일치하지 않음).
분자는 전기성이 다른 원소를 가질 수 있지만 메탄, CH4와 같이 비극성 일 수있다. 이것은 물을 극 (반대 전하의 극을 갖는) 분자로 만듭니다. 이로 인해 Ca2+, Mg2+, Na+, Cl- 등과 같은 미네랄은 용해됩니다 (물 분자의 음의 극은 양으로 하전 된 미네랄 이온을 끌어 들이고 그 반대로). 이 이온은 전위차가있는 경우 전기를 전도 할 수 있습니다 .
또한, 분자간 결합은 분자간 수소 결합으로 인해 물에서 강하다. 알코올에 비해 물의 끓는점이 높은 이유입니다.
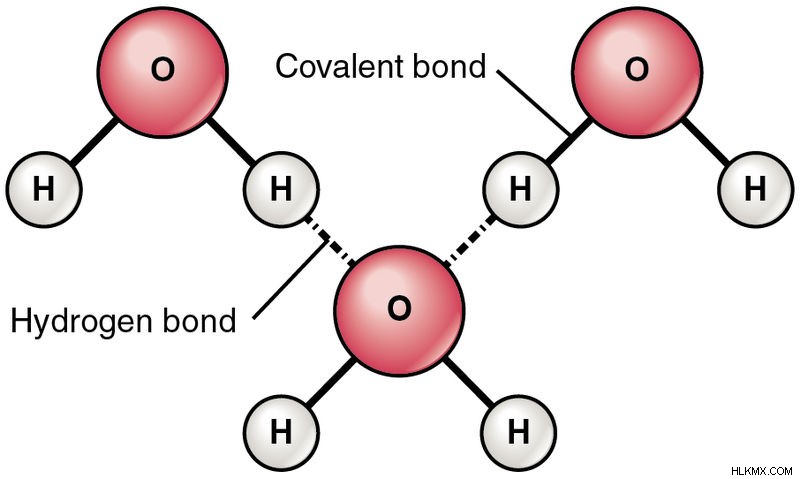
공유 및 수소 결합을 보여주는 물 분자의 구조적 공식 (사진 크레디트 :OpenStax College
/wikimedia commons)
알코올 화학
공통적으로 알코올은 의료 목적으로 주류 또는 액체를 말합니다. 그러나 과학에서 알코올은 단일 액체가 아니라 기능적 그룹 을 갖는 유기 (즉, 탄소 함유) 화합물의 종류입니다. (-오). 기능적 그룹은 원자의 수집으로, 일부 독특한 특성이 그것에 결합 된 유기 화합물과 관련이 있습니다.
물의 경우와 마찬가지로, 원소 사이에 형성된 결합은 공유 결합 (전자 공유)이다. 이것은 전기를 전도하기 위해 유리 전자와 이온의 부족으로 해석됩니다. 따라서 순수한 알코올은 또한 절연체입니다.
알코올에 미네랄 이온을 용해시키는 것은 탄소 사슬과 미네랄 이온 사이에 세기적 방해 (기존 종의 반발로 인한 새로운 종을 수용하는 데 어려움)가 있기 때문에 물에 용해시키는 것보다 더 어려워집니다. 전하의 크기는 알코올에서도 적습니다.
고도로 전기 음성 O는 한쪽 끝에 부착되므로 전자 쌍을 그 자체로 끌어 당겨 부분적 음전하를 얻고 다른 원자에 부분 양전하를 제공합니다. 알코올은 극 끝 (-OH) 및 비극성 말단 (탄소 사슬)을 갖는 것으로 시각화 될 수 있습니다. 이것은 알코올을 양서류 화합물로 만듭니다 (극성 및 비극성 화합물과 비극성 화합물과 결합하는 데 적합). 클렌징 및 소독 모두에 적용됩니다.
또한 알코올의 분자간 인력은 물보다 약합니다 (부피가 큰 탄소 사슬의 존재로 인한 입체 방해). 따라서 물보다 알코올을 증발시키는 것이 입니다 .
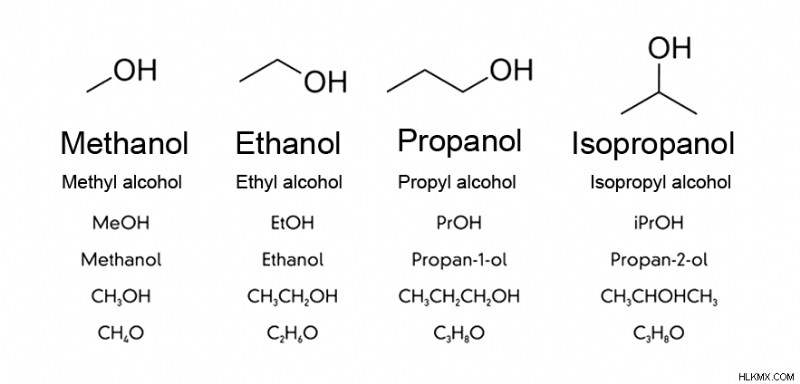
스틱은 탄소 사슬을 나타내고 -oh는 기능 그룹입니다 (사진 크레디트 :Peter Hermes Furian/Shutterstock)
전자 제품에 대한 물의 영향
전자 제품과 접촉하는 물의 결과는 단기 및 장기 효과의 두 부분으로 나눌 수 있습니다.
물에는 용해 된 미네랄 이온이 포함되어 있기 때문에 전기를 전도 할 수 있습니다. 구동 장치가 물과 접촉하면 장치 내부의 여러 터미널이 동일한 도체, 즉 물과 접촉합니다. 전류 흐름에 대한 대체 경로가 생성되고 전기가 안되는 방향으로 전기가 흐르기 시작합니다. 이것을 단락이라고합니다. 단락 동안, 엄청난 양의 전류 흐름이 짧은 시간 내에 발생하여 과도한 가열이 발생하고 최악의 경우 화재!
대부분의 장치는 DC 배터리를 전원으로 사용하기 때문에 양극과 접촉하는 물과 배터리의 음극은 가연성 H2 및 O2 가스의 진화로 전기 분해로 이어질 것입니다.
물은 또한 용존 산소 (O2) 분자를 함유하고 있습니다. 모든 전자 장치에는 PCB (인쇄 회로 보드)가 포함되어 있습니다. PCB에는 지휘자로 구리, 금 및 팔라듐과 같은 금속이 있습니다. 물에 노출 될 때, 산화 환원 반응은 금속이 전자를 잃고 금속 산화물 층을 형성하는 경우에 산화 환원 반응이 발생한다. 초과 근무로, 이로 인해 터미널에서 전도성 금속의 부피가 감소합니다 (분해). 극단적 인 경우 금속이 구조적으로 약해져 부서집니다.
LED/LCD 디스플레이 화면에는 조명을 제공하는 백라이트 패널이 포함되어 있습니다. 물이 백라이트 패널에 들어가면 조명의 부적절한 굴절이 발생하고 결과 디스플레이가 왜곡됩니다 (흐릿한 모양, 검은 반점 등).

부식 손상된 반도체 (사진 크레디트 :이진 시퀀스/Wikimedia Commons)
또한, 물 분자는 스피커를 차단하여 머플러 출력을 초래할 수 있습니다.
전자 제품에 대한 알코올 효과
알코올은 물에서 발견되는 것만 큼 높은 농도로 용해 된 이온 성 불순물을 포함하지 않습니다. 알코올이 전자 제품과 접촉하면 자유 하전 종 (이온 및 유리 전자)의 부족은 전도도에 영향을 미치지 않습니다. 따라서 단락이 발생하지 않습니다.
알코올은 물보다 빠르게 증발하기 때문에 전자 성분에 손상을 줄 수있을 정도로 알코올이 오래 걸릴 가능성이 제거됩니다. 따라서 디스플레이와 스피커가 망가질 확률은 감소합니다.
더욱이, 알코올은 극성 및 비극성 화합물에 결합 할 수 있기 때문에, 알코올은 친 유성 세균의 지방 세포막에 결합하고 또한 미생물로 단백질을 거부하여 효과적으로 죽인다. 따라서 알코올 (특히 이소 프로필 알코올, IPA)은 종종 세척제로 사용됩니다.

이소 프로필 알코올은 널리 사용되는 세정제입니다 (사진 크레디트 :20)
최종 단어
위의 논의는 주로 식수 및 저 분자 체중 알코올 (에탄올, 이소 프로필 알코올 등)을 중심으로 진행되었습니다. 순수한 물과 순수한 알코올은 거의 전자 장치를 손상시키지 않지만, 용해 된 불순물과 분자간 결합은 일이 잘못 될 때 주요 범인입니다! 기본적으로 물은 알코올보다 더 많은 불순물을 용해시키고 증발 할 수 있기 때문에 알코올보다 전자 장치를 더 쉽게 망치는 경향이 있습니다.