물의 동결 지점을 알고 있습니까? 동결 지점이 녹는 점과 동일합니까? 다음은 동결 지점의 온도, 영향을 미치는 요인 및 용융점과 동일인지 여부를 살펴 봅니다.
수의 정상 동결 지점의 온도
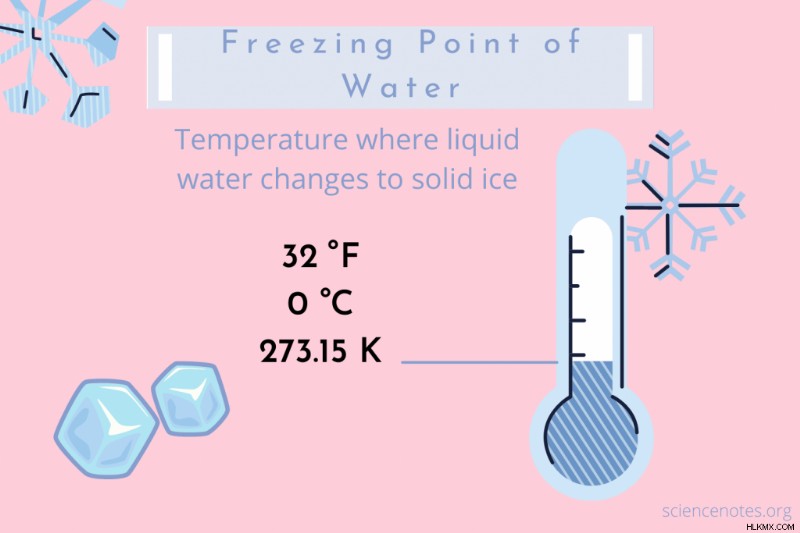
물의 동결 지점의 온도는 32 ° F, 0 ° C 또는 273.15 k 입니다. . Kelvin 온도에는 켈빈 스케일이 절대 온도 스케일이기 때문에 켈빈 온도에는 학위 기호가 부족합니다. 이것은 액체 물이 1 개의 압력 대기에서 고체 얼음이되기 위해 위상 전이를 겪는 온도입니다.
동결 지점과 용융점의 차이
동결 지점은 액체가 고체로 변하는 온도 인 반면, 용융점은 고체가 액체로 변하는 온도이다. 대부분의 실제 목적을 위해 두 온도는 동일합니다. 따라서 물의 용융점은 또한 32 ° F, 0 ° C 또는 273.15 k입니다.
때로는 순수한 물의 동결 지점이 정상적인 동결 지점 또는 용융점보다 훨씬 낮을 수 있습니다. 그 이유는 물을 냉각하기가 쉽기 때문입니다. 과냉각수는 불순물, 기포 또는 표면 결함이없는 물로 결정 형성을 허용합니다. 부드러운 용기의 매우 순수한 물은 고체를 얼리기 전에 -40 ~ -42 ° F (-40 ° C)의 낮은 온도에 도달 할 수 있습니다!
동결 지점을 변경할 수있는 요인
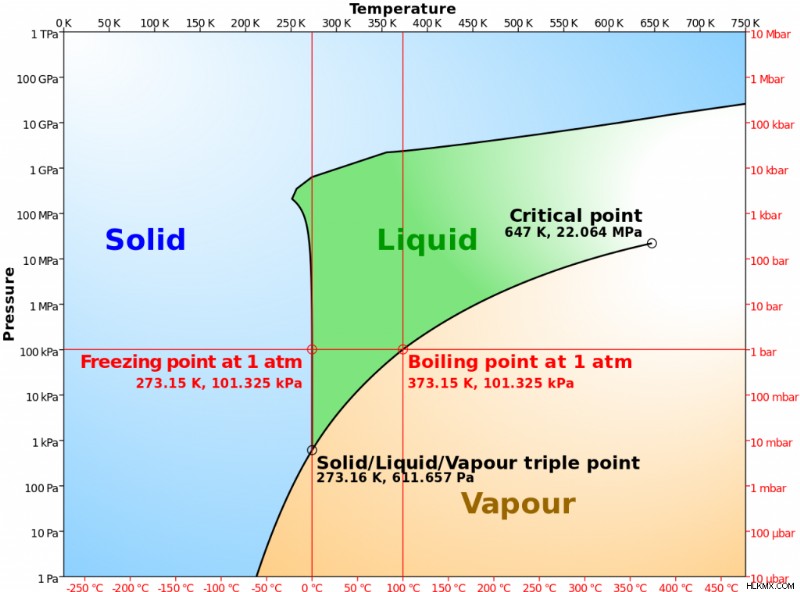
위상 다이어그램을 보면 동결 점 온도가 압력에 따라 다릅니다. 대부분의 물질의 경우 1 대기 미만의 압력 감소는 동결 지점을 낮 춥니 다. 그러나 반대는 물에서 발생합니다. 처음에는 압력을 높이면 얼어 붙은 점이 낮습니다. 그 이유는 물 분자 사이의 수소 결합이 액체를 고체보다 밀도가 높고 매우 안정적으로 만들기 때문입니다. 매우 낮은 압력, 물은 액체가되지 않고 수증기에서 얼음으로 직접 변합니다.
불순물은 또한 물의 동결 지점에 영향을 미칩니다. 거의 모든 경우에, 물질 (예 :설탕, 소금, 알코올)을 용해시키는 것은 동결 지점을 낮 춥니 다. 이것을 동결 지점 우울증이라고합니다. 물질의 공동 특성이므로 입자의 화학적 특성이 아니라 물에 첨가 된 입자의 수에 따라 다릅니다. 리즈 대학교 (University of Leeds)의 과학자들은 얼어 붙는 지점 우울증에 대한 예외를 발견했습니다. 소금 인 황산 암모늄은 실제로 물의 동결 지점을 올립니다.
먼지 나 꽃가루와 같이 물에 녹지 않는 입자도 물의 동결 지점을 높입니다. 입자는 핵 생성 지점으로서 작용한다. 기본적으로, 그들은 물 분자에게 결정화 과정을 얼음으로 시작하기 위해 부착 지점을 제공합니다. 스키 리조트는이 속성을 사용하여 얼어 붙은 온도에서 눈을 만듭니다.
참조
- Atkins, P.W. (2017). 물리 화학의 요소 . ISBN 978-0-19-879670-1.
- Pedersen, U.R.; et al. (2016 년 8 월). "동결 및 용융의 열역학". 자연 통신 . 7 (1) :12386. doi :10.1038/ncomms12386
- Zachariassen, K.E.; Kristiansen, E. (2000 년 12 월). “자연의 얼음 핵 생성 및 항 핵 생성”. cryobiology . 41 (4) :257–79. doi :10.1006/cryo.2000.228