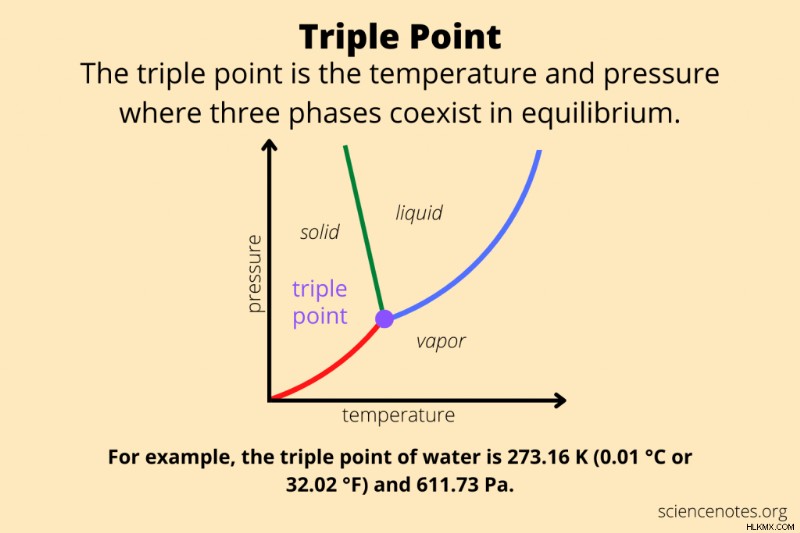
화학 및 물리학에서 트리플 포인트 순수한 물질의 것은 열역학적 평형에 3 상이 존재하는 온도와 압력의 조합이다. 일반적으로 트리플 포인트는 물질의 고체, 액체 및 증기 상이 평형에서 공존하는 지점을 나타냅니다. 그러나이 용어는 또한 3 단계가 공존하는 온도와 압력에도 적용됩니다. 따라서 물질에 다수의 고체 상 (결정 구조)이 있으면 다수의 트리플 포인트 값이 있습니다.
물의 트리플 포인트
사람들은 종종 물의 트리플 포인트 온도를 말하지만 트리플 포인트는 실제로 온도와 압력의 조합입니다. 물의 트리플 포인트는 273.16 켈빈 (0.01 ° C 또는 32.02 ° F)과 611.7 파스칼 (6.117 millibars, 0.0060373057 atm)의 압력입니다. (일부 소스는 611.73 PA의 압력을 나열하고 다른 소스는 611.657 PA의 압력을 인용합니다.)이 시점에서 얼음, 물 및 수증기는 안정적인 형태로 공존합니다. 온도 또는 압력의 가장 작은 변화는 물이 얼음, 액체 물 및 수증기 사이의 형태를 변화시킵니다.
시스템의 총 압력은 트리플 포인트의 압력보다 훨씬 높을 수 있으며, 물의 부분 압력은 611 pa에 있습니다. 또한 트리플 포인트는 액체 물이 존재하는 가장 낮은 압력에 해당합니다. 이 압력 아래에서 얼음은 직접 증기로 변환되고 증기는 얼음으로 승화됩니다.
일반적으로 트리플 포인트는 물질의 액체 형태가 존재할 수있는 최소 온도입니다. 압력의 함수 (적어도 육각형 얼음의 경우)로 용융점이 감소하는 방식 때문에 물은 이와 관련하여 드문 일입니다.
.공통 물질에 대한 트리플 포인트 값의 표
이 표에는 여러 순수한 물질에 대한 트리플 포인트 값이 나열되어 있습니다. 대부분의 데이터는 NIST (U.S. National Institute of Standards and Technology)에서 비롯되며 Donner et al. 및 Hoffer et al. 트리플 포인트 값은 일반적으로 "6 나인"순도를 갖는 샘플의 검사에서 비롯됩니다. 다시 말해, 샘플은 99.9999% 순수합니다.
| 물질 | 온도 k (° C) | 압력 kpa (atm) |
|---|---|---|
| acetylene | 192.4 k (-80.7 ° C) | 120 kPa (1.2 atm) |
| 암모니아 | 195.40 k (-77.75 ° C) | 6.060 kPa (0.05981 atm) |
| argon | 83.8058 k (-189.3442 ° C) | 68.9 kPa (0.680 atm) |
| arsenic | 1,090 k (820 ° C) | 3,628 kPa (35.81 atm) |
| butane | 134.6 k (-138.6 ° C) | 7 × 10 kPa (6.9 × 10 atm) |
| Carbon (graphite) | 4,765 k (4,492 ° C) | 10,132 kPa (100.00 atm) |
| 이산화탄소 | 216.55 k (-56.60 ° C) | 517 kPa (5.10 atm) |
| 일산화탄소 | 68.10 k (-205.05 ° C) | 15.37 kpa (0.1517 atm) |
| chloroform | 175.43 k (-97.72 ° C) | 0.870 kPa (0.00859 atm) |
| 중수소 | 18.63 k (-254.52 ° C) | 17.1 kpa (0.169 atm) |
| Ethane | 89.89 k (-183.26 ° C) | 1.1 × 10 kPa (1.1 × 10 atm) |
| ethanol | 150 k (-123 ° C) | 4.3 × 10 kPa (4.2 × 10 atm) |
| 에틸렌 | 104.0 k (-169.2 ° C) | 0.12 kPa (0.0012 atm) |
| 포름 산 | 281.40 k (8.25 ° C) | 2.2 kPa (0.022 atm) |
| helium-4 (lambda point) | 2.1768 k (-270.9732 ° C) | 5.048 kPa (0.04982 atm) |
| helium-4 (hcp-bcc-he-ii) | 1.463 K (-271.687 ° C) | 26.036 kPa (0.25696 atm) |
| helium-4 (bcc-he-1-he-ii) | 1.762 K (-271.388 ° C) | 29.725 kPa (0.29336 atm) |
| helium-4 (hcp-bcc-he-1) | 1.772 k (-271.378 ° C) | 30.016 KPA (0.29623 atm) |
| hexafluoroethane | 173.08 k (-100.07 ° C) | 26.60 kPa (0.2625 atm) |
| 수소 | 13.8033 k (-259.3467 ° C) | 7.04 kPa (0.0695 atm) |
| 수소 클로라이드 | 158.96 k (-114.19 ° C) | 13.9 kPa (0.137 atm) |
| iodine | 386.65 k (113.50 ° C) | 12.07 kPa (0.1191 atm) |
| isobutane | 113.55 k (-159.60 ° C) | 1.9481 × 10 kPa (1.9226 × 10 atm) |
| krypton | 115.76 k (-157.39 ° C) | 74.12 kpa (0.7315 atm) |
| Mercury | 234.3156 k (-38.8344 ° C) | 1.65 × 10 kPa (1.63 × 10 atm) |
| methane | 90.68 k (-182.47 ° C) | 11.7 kpa (0.115 atm) |
| neon | 24.5561 k (-248.5939 ° C) | 43.332 kpa (0.42765 atm) |
| Nitric Oxide | 109.50 k (-163.65 ° C) | 21.92 kPa (0.2163 atm) |
| 질소 | 63.18 k (-209.97 ° C) | 12.6 kPa (0.124 atm) |
| 아산화 질소 | 182.34 k (-90.81 ° C) | 87.85 kPa (0.8670 atm) |
| 산소 | 54.3584 K (-218.7916 ° C) | 0.14625 kpa (0.0014434 atm) |
| palladium | 1,825 k (1,552 ° C) | 3.5 × 10 kPa (3.5 × 10 atm) |
| platinum | 2,045 k (1,772 ° C) | 2 × 10 kPa (2.0 × 10 atm) |
| radon | 202 k (-71 ° C) | 70 kPa (0.69 atm) |
| 이산화황 | 197.69 k (-75.46 ° C) | 1.67 kPa (0.0165 atm) |
| titanium | 1,941 k (1,668 ° C) | 5.3 × 10 kPa (5.2 × 10 atm) |
| Uranium hexafluoride | 337.17 k (64.02 ° C) | 151.7 kpa (1.497 atm) |
| water | 273.16 k (0.01 ° C) | 0.611657 KPA (0.00603659 atm) |
| Xenon | 161.3 k (-111.8 ° C) | 81.5 kPa (0.804 atm) |
| incl | 692.65 k (419.50 ° C) | 0.065 kPa (0.00064 atm) |