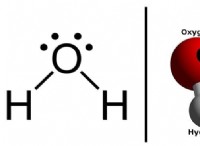
무거운 물은 중수소 산화물로도 알려져 있으며 화학 요소입니다. 수산화물에는 H라는 상징이 있고 1이라고 불리는 여러 원자가 있습니다. 체중에 관해서는 수소가 가장 가벼워집니다. 일반적으로, 수소는 공식 H2를 갖는 분자로 구성된 가스이다. 냄새가 나지 않고 독성이없고, 아무것도 보이지 않으며, 매우 가연성이 있습니다. 수소는 우주에서 가장 일반적인 화학 요소입니다. 그것은 우리 주변에서 볼 수있는 모든 일반적인 것들의 약 75%를 구성합니다. 많은 수소가 태양의 혈장 형태로 발견되어 빛납니다. 지구의 거의 모든 수소는 물과 같은 분자와 식물과 같은 유기 물질의 형태입니다.
헤비 워터 준비
-
헤비 워터의 다단계 전기 분해
수산화물은 물이 전해질되면 중수소보다 빠르게 방출되지만 중수소만큼 빠르지는 않습니다. 결과적으로, H2O 채권은 D2O 결합보다 18 배 더 자주 파괴됩니다. 약간의 물만 남을 때까지 전기 분해를 유지하면 나오는 D2O는 순수합니다. 우리가 30 리터의 물을 전해 할 때, 우리는 약 1ml (약 1 큰술)의 무거운 물을 얻었습니다.
-
교환 반응
D2O를 일종의 무거운 물로 만드는 방법도 있습니다. 예를 들어, H2S 가스가 가열 된 물을 통과 할 때 발생합니다. 이미 물에있는 D2O의 중수소 원자는 H2S의 수소 원자를 대체하는 데 사용되므로 물은 동일하게 유지됩니다. 따라서 D2S는 H2S에 넣습니다. H2를 중수소 및 냉수와 혼합하면 D2S의 중수소와 H2O의 수소가 다시 장소를 변경합니다. 과정이 반복되고 냉수는 매번 조금 더 D2O를 얻습니다.
-
분수 증류
분수 증류 공정은 무거운 물이 정상 물에서 얼마나 잘 분리되는지에 영향을 줄 수 있으므로 작동하지 않을 수 있습니다. 이 단계에서는 심각한 물의 끓는점의 차이가 사용됩니다. 따라서 가벼운 부분이 먼저 분해되어 무거운 물이 풍부한 잔류 물 (D2O)을 남겨 둡니다.
헤비 워터의 특성
헤비 워터의 물리적 특성
무거운 물에는 일반 물과 같은 색, 냄새 또는 맛이 없습니다. 또한 움직일 수 있습니다. 그것은 다양한 물리적 특성을 가지고 있습니다. 그 중 일부는 다음과 같습니다.
- 헤비 워터는 물보다 더 우수한 끓는점, 최대 밀도 및 잠열 기화 열이 있습니다 (18 g). 헤비 워터는 물 (18 g)보다 엄청난 분자량 (20 g)을 가지므로 물리적 상수가 더 높습니다.
- 또 다른 점에 주목해야 할 것은 무거운 물이 물과 섞일 때 물보다 유전체 상수가 낮다는 것입니다.
- 무거운 물의 이온 화학 물질은 물에도 녹지 않으므로 잘 섞이지 않습니다.
헤비 워터의 화학적 특성
물은 물을 사용하여 모든 화학 공정에 사용될 수 있습니다. 무거운 물은 물보다 반응성이 떨어집니다. 헤비 워터 사용자는 물 사용자만큼 빠르게 반응하지 않을 수 있습니다. O -D 결합은 O -H 결합보다 빠르게 분리됩니다. O – D 연결이 더 안정적입니다.
- 중수 분해 :일부 무기 염은 물에 의해 분해 될 수 있지만 모든 것이 될 수는 없습니다. 이것을 소금 중수 분해라고하며, 무거운 물이 사용되면 같은 방식으로 발생합니다.
ALCL3 + 3D2O → AL (OD) 3 + 3DCL
BAS + 2D2O → BA (OD) 2 + D2S
- 금속의 작용 :중수는 나트륨 및 칼슘과 같은 금속과 반응하여 중수소 방출 및 무거운 알칼리를 제공합니다.
2NA + 2D2O → 2NAOD + D2
- 금속 산화물에 대한 작용 :일산화 나트륨 및 산화 칼슘과 같은 기본 산화물이 무거운 물과 혼합 될 때 발생합니다. 이것은 무거운 알칼리를 만듭니다
Na2O + D2O → 2Naod
- 비금속 산화물에 대한 작용 :중수산은 무거운 물이 삼산화 황, 디노 펜 독화물 등과 같은 산성 비 금속 산화물과 접촉 할 때 만들어집니다.
- 금속 질화물, 포스 파이드 및 탄산화물의 작용 :심한 질화가있는 암모니아로 무거운 물이 분해됩니다.
MG3N2 + 6D2O → 3mg (OD) 2 + 2nd3
- 소금 중수 자궁의 형성 :사람들은 무거운 물로 소금 중수소를 만듭니다. 그들은 소금이 무거운 물의 용액에서 결정화 될 때 만들어집니다. cuso4.5d2o 및 mgso4.7d2o는 소금 인 소금의 두 가지 예입니다.
- 교환 반응 :중수는 수소 원자가있는 많은 다른 것들과 반응하여 수소 원자의 일부 또는 전부를 중수소로 대체합니다. 화합물에 이온 수소 원자가있는 경우 교환 과정이 자발적으로 발생합니다.
NAOH + D2O → NAOD + HDO
HCL + D2O → DCL + HDO
- 생물학적 효과 :무거운 물은 식물과 동물이 더 천천히 자라게 만듭니다. 씨앗은 순수하고 무거운 물에서 자라지 않으며 작은 물고기는 죽습니다. 또한 D2O가 많은 물은 당신에게 나쁘다.
무거운 물 사용
- 무거운 물은 세균과 박테리아를 제거하는 데 사용됩니다.
- 사람들은 헤비 워터의 다른 것들과 교환하여 여러 옥시 야신의 구조와 기본성에 대해 알아 내기 위해 다른 것들과 교환하는 능력을 사용했습니다.
- 이것은 전기 분해 또는 금속 같은 나트륨과 반응하여 중수소로 만들어지는 방식입니다.
- 원자력 발전소에서 일하는 사람들은 에너지 흐름을 늦추기 위해 헤비 워터를 사용합니다. 우라늄 원자는 분리하기 위해 매우 느리게 움직이는 중성자가 필요하므로 거대해야합니다. 중성자는 무거운 물을 통해 흐르면서 느려져“중재자”역할을합니다.
- “헤비 워터”라고 불리는 추적자는 방향족 전자 유전 적 치환, 대사 활동 및 기타 것들과 같은 것들을 조사하는 데 사용됩니다.
결론
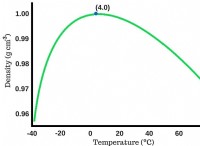
무거운 물인 D2O는 19311 년 Urey의 중수소 발견 이후 과학자들을 매료 시켰습니다. D2O의 밀도는 H2O보다 약간 밀도가 높습니다. 이것은 주로 중수소가 수소보다 무겁기 때문에 여전히 큰 차이입니다. 보다 미묘하게, 중수화는 수소 (또는 중수소) 결합을 H2O3,4 또는 H2O5, 6보다 D2O에서 더 강하게 만듭니다. 순수한 물이 중수화되면 PH (또는 PD)가 0.44만큼 변경됩니다.
이로 인해 각각 동결 및 비등점이 각각 3.8 ° C 및 1.4 ° C 증가합니다. 이것은 공기에서 CO2를 녹이고 열린 용기에 희석 된 탄산 산을 만드는 물에 해당되지 않습니다. 이것은 물의 pH에 훨씬 더 큰 영향을 미쳐 둘 이상의 단위로 변경합니다.