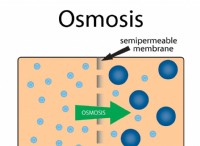
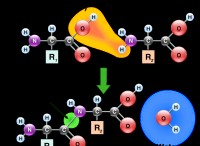
* 증발/비등 : 이것이 가장 일반적인 결과입니다. 액체가 에너지 (열)를 흡수함에 따라 분자는 운동 에너지를 얻고 더 빨리 움직입니다. 결국, 일부 분자는 액체 상태에서 그들을 붙잡고있는 세력을 극복하고 기체상으로 빠져 나갈 수있는 충분한 에너지를 가지고 있습니다.
* 증발 : 이것은 모든 온도에서 액체의 표면에서 발생합니다.
* 끓는 : 이것은 비등점이라는 특정 온도에서 액체 전체에 걸쳐 발생합니다.
* 동결 : 액체가 충분한 에너지를 잃으면 (냉각) 분자가 느려지고 움직임이 제한됩니다. 그들 사이의 매력은 더 강해져 분자가 더 질서가 있고 견고한 구조로 배열됩니다.
* 승화 : 경우에 따라 액체는 액체 상을 통과하지 않고 가스로 직접 전이 될 수있다. 이것은 액체가 이미 저압과 온도에있을 때 발생합니다. 예를 들어, 드라이 아이스 (고체 이산화탄소)는 실온 및 압력에서 이산화탄소 가스로 직접 승화시킨다.
특정 결과는 다음과 같습니다.
* 액체의 유형 : 각 액체에는 자체 끓는점과 동결 지점이 있습니다.
* 방출 된 에너지의 양 : 더 많은 에너지 방출은 액체 상태에서 더 큰 변화로 이어진다.
* 주변 압력 : 압력은 액체의 끓는점에 영향을 줄 수 있습니다.
예 :
* 물 : 물은 100 ° C (212 ° F)에서 끓고 표준 대기압에서 0 ° C (32 ° F)에서 동결됩니다.
* 에탄올 : 에탄올은 78.4 ° C (173 ° F)에서 끓고 -114 ° C (-173 ° F)에서 동결됩니다.
이러한 단계 변경 사항에 대한 자세한 내용을 원하시면 알려주세요!