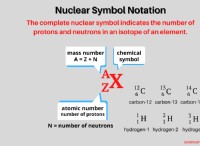
Selenocysteine (Sec) 및 Pyrrolysine (Pyl)은 20 개의 표준 아미노산만큼 널리 발생하지 않는 희귀 아미노산입니다.
대부분의 사람들은 단백질을 만드는 20 개의 아미노산이 있다는 것을 잘 알고 있지만, 그것이 실제로 거짓이라고 말하면 실제로 우리가 거의 이야기 할 수없는 몇 가지 추가 아미노산이 있습니다.
.
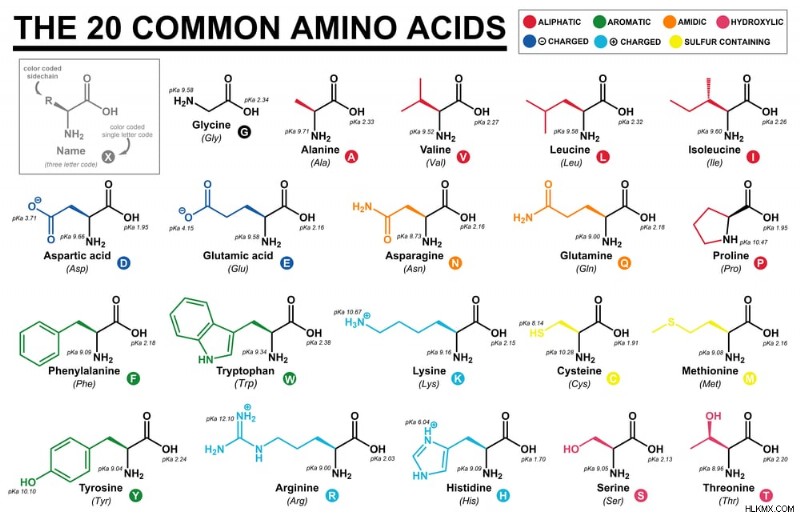
일반적인 아미노산 (사진 크레디트 :Cristian Victor Rete/Shutterstock)
총 22 아미노산 우리의 DNA에서 정의되었습니다. 셀레 노시 슈타인 (SEC) 및 피 롤리 신 (PYL)은 각각 21 번째 및 22 번째 아미노산이다. 그것들은 아미노산의 나머지 부분만큼 자연적으로 널리 퍼지지 않기 때문에 희귀 아미노산이라고합니다.
왜이 발견이 그렇게 충격적 이었습니까?
문자 A, G, T 및 C로 상징되는 4 개의 뉴클레오티드 염기는 우리 DNA 전체를 구성합니다. 1960 년대에 유전자 규범이 발견되었을 때 과학자들은 한 번에 3 개의 글자를 읽었다는 것을 발견했습니다. 이 세 글자는 공동으로 코돈으로 알려져 있으며 메신저 RNA (mRNA)에 존재합니다.
각각의 코돈은 단일 기능을 갖는 것으로 간주되었다 :20 개의 아미노산 중 하나를 나타내거나 (시작 코돈을 통해) 단백질 생성 번역 기계의 시작점 (정지 코돈을 통해)을 나타냅니다.
.
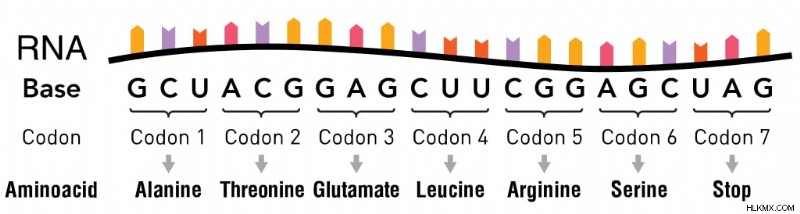
아미노산을 지정하고 정지 코돈에서 종료되는 mRNA에 대한 코돈 (사진 신용 :Thomas Splettstoesser/Wikimedia Commons)
이들 20 개의 아미노산은 모든 단백질의 골격이지만 일부 단백질은 다르거 나 비 전통적인 아미노산을 갖는다. 과학자들은 이들 아미노산의 대부분은 번역이 끝날 때 형성된 폴리펩티드 사슬이 형성된 후 구조가 바뀌는 원래 20에서 유래되었다. 이러한 변경 사항은 번역 후 변형 로 알려져 있습니다 그리고 단백질에 필요한 기능을 제공해야합니다.
이 아미노산은 드문 일이지만 여전히 중요한 기능이 있습니다. 예를 들어, 4- 하이드 록시 리신 및 5- 하이드 록시 프롤린은 각각 라이신과 프롤린의 유도체이며, 콜라겐 (결합 조직에서 발견 된 단백질)에서 발견된다.
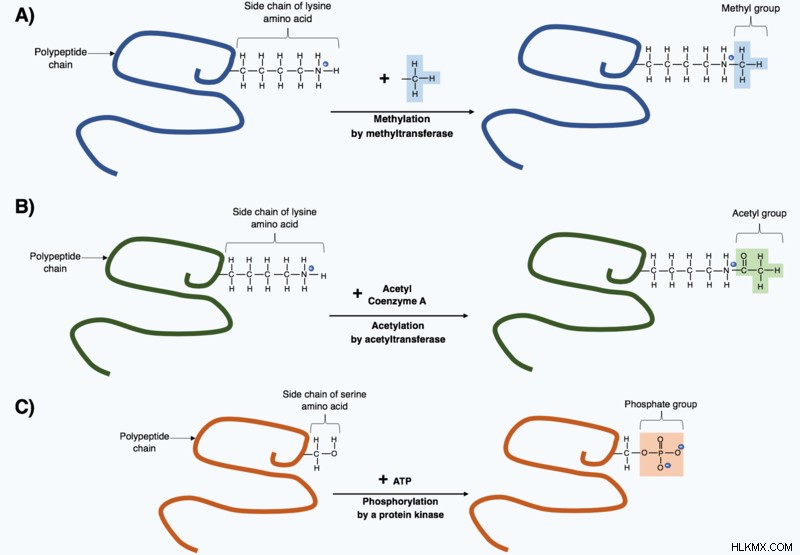
번역 후 수정 (사진 크레디트 :KEP17/Wikimedia Commons)
따라서, 셀레 노시 슈타인 (SEC) 및 피 롤리 신 (PYL)이 단백질에서 처음 발견 될 때, 이들은 각각 시스테인 및 라이신에 대한 변형 후 변형으로 인한 것으로 생각되었다. 그러나 1986 년에 두 가지 중요한 발견에 따르면 Selenocysteine은 실제로 STOP Codon UGA에 의해 코딩 된 것으로 나타났습니다. 16 년 후, Pyrrolysine은 STOP Codon UAG에 의해 코딩되는 것으로 확인되었습니다!
1960 년대 중반, 시작 코돈 (Aug)은 아미노산 메티오닌을 코딩 한 것으로 잘 알려져 있었지만, 정지 코돈 (UAG, UAA 및 UGA)은 단백질에 대해 코딩하는 것으로 여겨지지 않았지만 단순히 번역을 종식시켰다. 실제로, 그들은 아미노산을 형성하지 않기 때문에 말도 안되는 코돈이라고도했습니다.
따라서,이 발견은 정지 코돈에 새로운 역할을했기 때문에 획기적이었습니다. 또한, 두 가지 발견은 두 개의 별개의 유기체 인 e에서 개별적으로 이루어졌다. coli 및 마우스 - 이러한 특이한 아미노산이 다양한 종에 걸쳐 존재 함을 나타냅니다.
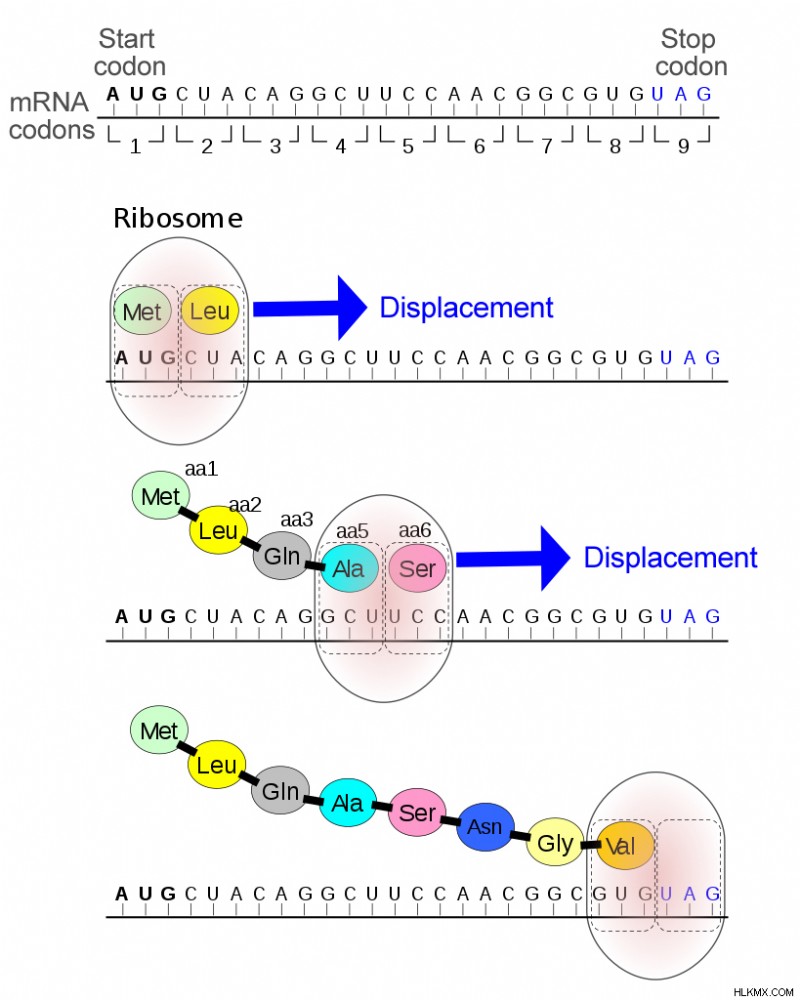
정지 코돈의 일반적인 메커니즘 (사진 크레디트 :Alain Gallien/Wikimedia Commons)
16 년 후, Pyrrolysine은 STOP Codon UAG에 의해 코딩되는 것으로 확인되었습니다!
왜 희귀 한가?
Selenocysteine (Sec) 및 Pyrrolysine (Pyl)은 DNA에서 코딩되지만 표준 아미노산과 달리 단백질에 포함되도록 특수 메커니즘이 필요합니다. 실제로, 이들은 두 개의 희귀 아미노산이 정지 코돈에 의해 코딩 되더라도 완전히 다른 메커니즘을 사용하여 그렇게하기 때문에 두 가지 메커니즘이 필요합니다.
피 롤리 신의 존재는 매우 제한된 수의 유기체에서 소수의 단백질로 제한된다. 지금까지, 전체 게놈 데이터를 이용할 수있는 약 1,000 개의 유기체의 11 개의 유기체만이 피로 리신을 인코딩합니다.
다른 한편으로, 셀레 노시 슈타인은 생명의 세 가지 도메인 (Archaea, Bacteria, Eukarya)에 걸쳐 많은 유기체에 존재한다. 시퀀싱 된 박테리아의 거의 4 분의 1에 의해 합성 된 것으로 여겨진다. 그러나 흥미롭게도, 17 개의 포유 동물 단백질만이 셀레 노시 슈타인을 합성하는 것으로 밝혀졌다.
중요합니까?
과학자들은 이미 많은 비표준 아미노산이 단백질에 통합되지 않을 수 있지만 여전히 수많은 대사 과정에서 중요한 중간체라는 것을 알고있었습니다. Selenocysteine과 Pyrrolysine은 실제로 DNA에 의해 코딩되기 때문에, 그것들은 필수적 일 가능성이 더 높았습니다. 그러나 희귀 성으로 인해이 두 아미노산의 중요성은 최근까지 간과되었습니다.
셀레 노시 슈타인은 시스테인과 구조적으로 유사하며 시스테인에서 발견되는 황 원자의 장소에 필수 미량 영양소 (Selenium)를 함유하고 있습니다. 그것은 셀레 노 단백질에서 발견되는 중요한 아미노산이며 다수의 대사 및 세포 과정과 관련이 있습니다. 뇌에서 셀레늄의 부족은 발작과 같은 신경 학적 이상을 유발하는 것으로 밝혀졌습니다. 그것은 신경 퇴행성 장애 외에도 여러 다른 질병과 관련이 있습니다. 그러나 연구자들은 아직 질병 메커니즘에서 정확한 역할을 식별하지 못했습니다.
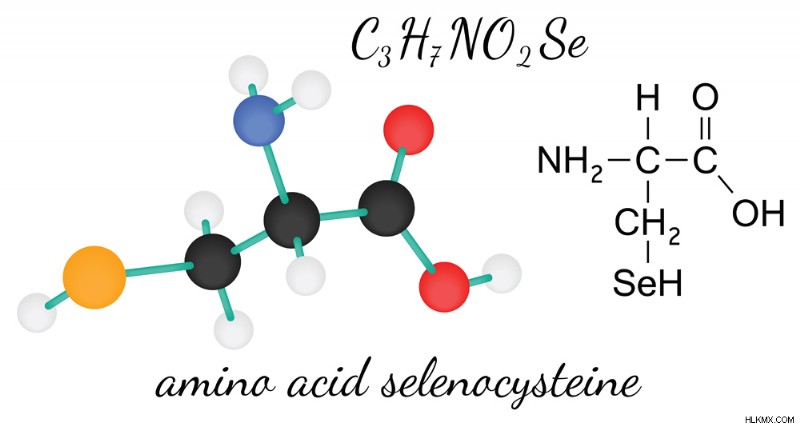
Selenocysteine의 구조 (사진 크레디트 :Shmitt Maria/Shutterstock)
피 롤리 신은 메타 노겐, 메타 노 사르시나 바 커리에서 확인되었다 소의 뱃속에서 찾을 수 있습니다! 최근까지, 피 롤리 신을 함유하는 단백질은 메탄 오겐에서만 발견되었으며, 이는 그것이 메탄 생산 (메탄 생성)에서 역할을한다는 것을 암시한다. 그것은 라이신과 구조적으로 유사하며 메탄 생성 동안 효소 메틸 트랜스퍼 라제를 도와줍니다. 피 롤리 산이 다른 과정에서 역할을하는지 확인하기위한 추가 연구가 필요합니다.
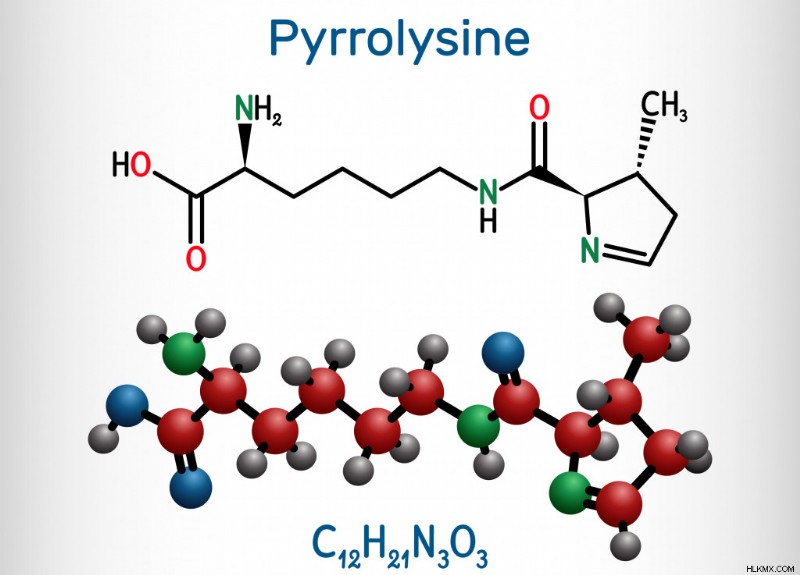
피 롤리 신의 구조 (사진 신용 :Bacsica/Shutterstock)
결론
생명의 진화 중에 왜 그리고 언제이 두 아미노산이 몇몇 유기체의 게놈에 첨가되었다. 그들은 현재 드문 것으로 분류되지만 추가 연구는 우리가 잘못을 증명할 수 있습니다. 결국, Albert Einstein의 말에 따르면,``우리는 여전히 자연이 우리에게 공개 한 것의 1 % 중 1 분의 1을 알지 못합니다.