코끼리와 다른 큰 동물은 통계적으로 예상되는 것보다 암 발병률이 낮으며, 이는 질병으로부터 자신을 보호 할 수있는 방법을 진화 시켰음을 시사합니다. 새로운 연구는 코끼리가 어떻게하는지 보여줍니다. 더 이상 기능적이지 않은 오래된 유전자는 방대한 "게놈 중 정크 야드"에서 재활용되어 코끼리 세포의 DNA 손상에 대한 민감도를 증가시켜 잠재적으로 암 세포를 조기에 끌어들일 수 있습니다.
.다세포 동물에서, 세포는 많은주기의 성장과 분열을 통과합니다. 각각의 분열에서, 세포는 전체 게놈을 복사하고 필연적으로 몇 가지 실수가 발생합니다. 이러한 돌연변이 중 일부는 암으로 이어질 수 있습니다. 신체가 더 큰 동물과 더 긴 삶을 가진 동물은 암 발병 위험이 더 큽니다. 그러나 그것은 연구자들이 광범위한 신체 크기에 걸쳐 종을 비교할 때 보는 것이 아닙니다. 암의 발병률은 유기체의 세포 수와 상관 관계가없는 것처럼 보이지 않습니다. 실제로, 연구자들은 더 크고 더 긴 포유류가 암 사례가 적다는 것을 발견했습니다. 1970 년대에 암 역학 학자 Richard Peto는 현재 옥스포드 대학교의 의료 통계 및 역학 교수 인 Richard Peto가 Peto의 역설로 알려진이 놀라운 현상을 표현했습니다.
.코끼리와 같은 더 큰 동물이 암의 비율이 높지 않다는 사실은 특수 암 억제 메커니즘을 진화 시켰음을 시사합니다. 2015 년 유타 대학교 의과 대학의 Joshua Schiffman과 Arizona State University의 Carlo Maley는 코끼리 게놈에 약 20 개의 추가 복제물이 p53 을 보여준 연구 팀을 이끌었습니다. , 표준 종양 억제 유전자. 그들은 p53 의 추가 사본을 제안했습니다. 코끼리의 강화 된 암 억제 능력에 대해 적어도 부분적으로 설명 할 수 있습니다. 현재이 연구에 기여한 유타 의과 대학의 세포 생물학자인 Lisa M. Abegglen은 p53 의 사본을 찾기위한 프로젝트를 이끌고 있습니다. 다른 기능이 있습니다.
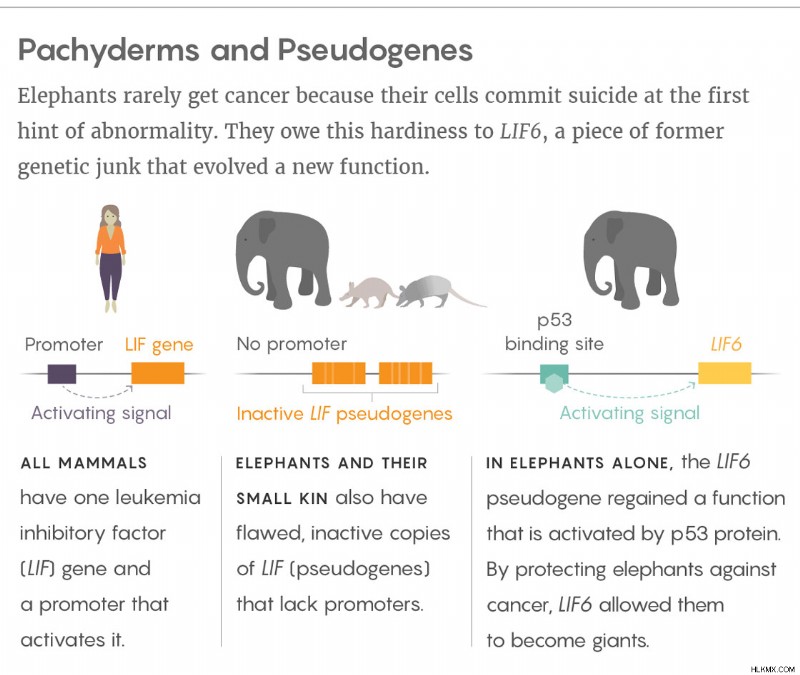
그러나 p53 의 추가 사본 코끼리의 유일한 보호 원이 아닙니다. 시카고 대학교 (University of Chicago)의 유전 학자 인 빈센트 린치 (Vincent Lynch)가 이끄는 새로운 작품은 코끼리와 소규모의 친척 (예 :hyraxes, armadillos 및 aardvarks)도 lif 의 복제본 사본도 가지고 있음을 보여줍니다. 백혈병 억제 인자를 암호화하는 유전자. 이 신호 전달 단백질은 일반적으로 생식력과 생식에 관여하며 배아 줄기 세포의 성장을 자극합니다. Lynch는 2017 년 8 월 캘거리에서 열린 Pan-American Society for Evolutional Developmental Biology Meeting에서 그의 작품을 발표했으며 현재 Biorxiv.org에 게시되었습니다.
.Lynch는 11 개의 LIF 의 복제물이 있음을 발견했습니다 서로 다르지만 모두 불완전합니다. 최소한 단백질 코딩 정보의 초기 블록과 유전자의 활성을 조절하기위한 프로모터 서열이 부족합니다. 이러한 결함은 린치에게 중복이 lif 의 정상적인 기능을 수행 할 수 없다고 제안했다. 유전자 또는 심지어 세포에 의해 발현됩니다.
그러나 Lynch가 세포를 보았을 때, 그는 적어도 하나의 복제물에서 RNA 전 사체를 발견했습니다. lif6 , 이는 프로모터 시퀀스가 켜져 있어야한다는 것을 나타냅니다. 실제로, lif6 의 상류에 수천 개의베이스가 있습니다 게놈에서 Lynch와 그의 공동 작업자는 p53 단백질의 결합 부위처럼 보이는 일련의 DNA를 발견했습니다. 그들에게 p53 을 제안했다 ( p53 중 어느 것도 아닙니다 복제)는 lif6 의 발현을 조절할 수있다 . 코끼리 세포에 대한 후속 실험은이 직감을 확인했습니다.
lif6 을 발견합니다 연구원들은 유전자의 활동을 차단하고 세포를 DNA 손상 조건에 적용했습니다. 그 결과 세포는 아 pop 토 시스 (프로그램 된 세포 사멸)라는 과정을 통해 자신을 파괴 할 가능성이 줄어들 었으며, 이는 유기체가 종종 결함있는 조직을 제거하기위한 일종의 품질 관리 시스템으로 사용합니다. lif6 따라서 잠재적으로 악성 세포를 근절하는 데 도움이되는 것 같습니다. 추가 실험은 lif6 을 나타냈다 미토콘드리아 주변의 막에 누출을 생성하여 세포 사멸을 유발합니다.
lif 의 진화 역사에 대해 자세히 알아 보려면 그리고 그 복제물 인 Lynch는 Manatees, hyraxes 및 멸종 된 Mammoths 및 Mastodons와 밀접하게 관련된 종의 게놈에서 상대방을 발견했습니다. 그의 분석은 lif 을 제안했다 유전자는 17 번 복제되었고 코끼리 계보가 진화하는 동안 14 회 손실되었습니다. Hyraxes와 Manatees는 lif 을 가지고 있습니다 복제이지만 p53 복제는 살고 멸종 된 코끼리에서만 나타나며, 이는 lif 을 시사합니다. 복제는 진화에서 일찍 발생했습니다.

Lynch는 LIF의 대부분의 복제물을 발견했습니다 유전자는 우연히 게놈에서 생존하는 오래되고 돌연변이, 쓸모없는 유전자 카피입니다. 그러나 예외는 lif6 입니다 다른 사람들이 무작위 돌연변이를 축적하지 않은 유전자 서열은 자연 선택이 그것을 보존한다는 것을 암시한다.
“우리는 lif6 이라고 생각합니다 린치는 말했다. 즉, 코끼리 lif6 입니다 유사 유전자 조상으로부터 기능성 유전자로 다시 진화했다. Lynch는 죽음에서 돌아와서 세포 죽음에서 역할을하기 때문에 그것을“좀비 유전자”라고 불렀습니다.
Manatees와 Hyraxes에는 추가 사본이 있습니다. , 현대적이고 멸종 된 코끼리 만 lif6 을 가지고 있습니다 코끼리가 관련 종에서 멀어진 후에 만 진화했음을 시사합니다. Lynch의 그룹이 Lif6 의 기원을 날렸을 때 분자 클록 방법에 의해, 그들은 화석 기록이 코끼리가 큰 신체 크기를 진화하고 있음을 나타내는 약 3 천만 년 전에 유사 유전자가 기능을 되찾았다는 것을 발견했다.
.
Yale University의 진화 생물 학자 인 Stephen Stearns는“유사 유전자를 환불하는 것은 매일 일어나는 일이 아닙니다. . 그는 코끼리가 큰 몸을 진화시키는 동시에 일어났다는 것을 보여줄 수 있다는 것을 보여줄 수 있다는 사실을 보여줄 수 있다는 것은“유전자의 환급이 큰 신체 크기의 진화를위한 전제 조건임을지지하지만 증명하지는 않는다”고 썼다.
암에 대한 진화하는 보호는 모든 동물의 관심에있는 것처럼 보일 것입니다. 왜냐하면 그들은 모두 수반 된 lif6 을 가지고 있지 않습니까? 유전자? 연구원들에 따르면,이 보호에는 위험이 발생하기 때문입니다. lif6 암을 억제하지만 lif6 의 추가 사본 그들이 우연히 켜면 셀을 죽일 것입니다. 린치는 이메일로 설명했다. "부적절하게 표현되면 기본적으로 게임 오버입니다."
또한 암 억제 메커니즘과 다산 사이에 상충 관계가있는 것으로 보입니다. 2009 년에 발표 된 연구에 따르면 LIF 이 제안되었습니다 자궁 내 배아의 이식에 중요합니다. lif 때문입니다 활동은 p53 에 의해 제어됩니다 , lif 및 p53 생식의 효율성을 공동으로 조절합니다. 동일한 유전자 세트에 두 가지 기능 (생식 및 암 억제와 같은)이있을 때, 그러한 기능이 직접적인 갈등에있을 가능성이 있습니다.
코끼리는 복제 p53 를 복제함으로써 길항 적 다이오 엇의 문제를 해결했을 수있다. 및 LIF Maley에 따르면 이러한 기능을 분할합니다. “ p53 의 일부 사본 및 LIF 다산에 필요한 일을하고 있지만 다른 쌍의 lif 및 p53 암 억제에 필요한 일을하고 있습니다.”라고 그는 말했다. Maley는 유전자가“코끼리가 암 억제에 더 잘 어울리고 여전히 생식력을 유지하여 더 큰 몸을 키울 수있게 해줄 수있게 해주었다”고 추측했다. 그러나 그 가설은 여전히 테스트되어야한다고 그는 말했다.
p53 의 추가 사본 및 LIF 코끼리가 Peto의 역설을 극복하는 데 도움이되었지만 유일한 해결책이 될 수는 없습니다. 고래와 같은 다른 큰 동물은 p53 의 사본이 하나뿐입니다. lif 의 한 버전 . Lynch와 그의 팀은 현재 고래와 박쥐가 Peto의 역설을 어떻게 해결하는지 탐구하고 있습니다. 대지가 크지는 않지만 일부 박쥐 종은 최대 30 년까지 살고 있으며, 더 많은 종은 더 짧은 수명이 부족한 암 억제 메커니즘을 진화시킬 수 있습니다.
Maley는 또한 고래가 Peto의 역설을 해결하는 방법에 대해서도 노력하고 있습니다. 고래에는 p53 의 추가 사본이 없지만 그는“우리는 p53 의 유전자에 대한 많은 선택과 진화가 있다고 생각합니다. 좁은 길." Maley는 다양한 대형 동물 동물이 PETO의 역설을 해결하는 방법을 이해하면 인간 건강에 적용될 수 있다고 생각합니다. "이것이 최종 목표"라고 그는 말했다. "희망은 진화가 어떻게 암을 예방하는 방법을 찾아서, 우리는 그것을 인간의 암 예방으로 더 나은 암 예방으로 번역 할 수 있기를 바랍니다."
.Maley는“큰 신체 크기를 진화시킨 모든 유기체는 아마도 Peto의 역설에 대한 다른 해결책을 가지고있을 것입니다. "자연에서 우리를 기다리고있는 많은 발견이 있습니다. 자연은 우리에게 암을 예방하는 방법을 보여줍니다."
.