알코올의 –oh 그룹의 알킬 그룹으로 h를 대체한다.
CH3CH2-OH ⇒ ch3ch2-o-r
이 화합물을 에테르라고합니다.
에테르는 산소 원자에 의해 연결된 2 개의 알킬기를 갖는 유기 화합물이다. 에테르의 일반적인 공식은
입니다r -o -r '
여기서 r과 r '은 알킬 또는 아릴입니다.
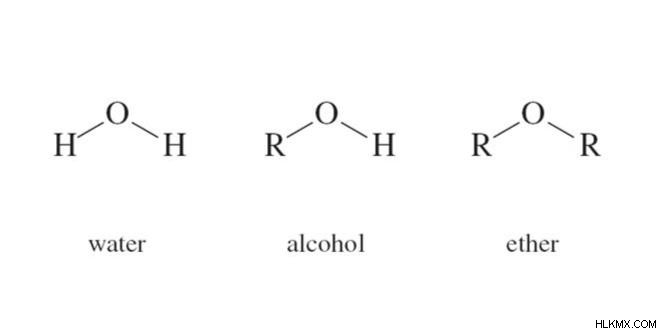
에테르의 예 :
아래는 몇 가지 에테르 예를 제시했습니다.
1. CH3 - O - CH3 (디메틸 에테르)
2. (CH3) 2CH - OCH (CH3) 2 (디 이소 프로필 에테르)
3.
와 같은 순환 에테르c6h5-o-c6h5 (디 페닐 에테르)
에테르의 준비 :
-
에테르의 기능적 그룹은 c-o-C입니다. 중심 원자 산소는 SP3 하이브리드 화 상태에 있습니다.
-
이것들은 일반 사면체의 네 모서리를 향하고 서로 109 ° 28 ′의 각도를 만듭니다.
-
SP3 하이브리드 궤도 사이의 각도는 109 ° 28 ′
입니다. -
각 SP3 하이브리드 궤도는 25% S 및 75% P 문자입니다.
-
나머지 두 개의 SP3 궤도는 자유롭지 않습니다. 즉, 그들은 궤도와의 결합을 형성하지 않습니다. 여기서, C-O-C 결합 각도는 약 110 °이며, 이는 정상 사면체 (109 ° 28 ′)에 가깝고 물 (105 °)과 다릅니다.
.
-
이 차이는 에테르에서 전자 쌍의 고독한 쌍의 반발은 부피가 큰 알킬 그룹 사이의 반발에 의해 균형을 잡기 때문에 109 ° 28 '근처의 결과 값이 유지되기 때문입니다.
.
에테르의 기하학적 부분
-
에테르는 대칭이거나 단순 할 수 있으며 (알킬 그룹이 동일 할 때) 비대칭 또는 혼합 (두 알킬 그룹이 다를 때).
대칭 에테르의 예
CH3 - CH2 - O - CH2 - CH3 (디 에틸 에테르)
비대칭 에테르의 예
CH3 - O - CH2 - CH3 (에틸 메틸 에테르)
-
에테르는 기능적 이성질체 (알코올 포함)와 메타 미러를 보여줍니다.
-
에테르로 알려진 디 에틸 에테르 (에 톡시 에탄)가 가장 중요한 예입니다.
에테르의 물리적 및 화학적 특성
화학적 특성 :
-
에테르는 가연성입니다.
-
디 에틸 에테르는 비등점이 35o c이므로 플래시 화를 낼 위험입니다.
-
에테르는 공기로부터의 산소와 천천히 반응하여 불안정한 히드로 로산화수소와 퍼 옥사이드를 형성하여 폭발 위험을 나타냅니다.
r-o-o-h (히드로 로산화물)
r-o-o-r (퍼 옥사이드)
-
에테르는 산, 염기 및 산화제에 대해 반응하지 않기 때문에 적합한 용매를 만듭니다.
-
알칸과 마찬가지로 아테네는 연소 및 할로겐화 반응을 겪습니다.
물리적 특성 :
-
에테르는 무색이며 낮은 비등 지점의 고 풍선 화합물입니다.
-
화학적 비 활동과 지방, 오일, 잇몸 및 기타 유기 화합물을 용해시키는 능력이 우수한 용매를 만듭니다.
-
에테르는 황산에 용해됩니다. 이 특성은 에테르와 포화 탄화수소 사이의 저명한 테스트로 사용됩니다.
-
하부 에테르는 마취제로 작용합니다.
-
에테르는 물보다 가볍습니다.
명명법 IUPAC ETHERS의 이름 :
IUPAC 규칙을 사용하여 에테르를 명명하는 동안, 더 복잡한 그룹은 루트 이름으로 사용되며 산소 원자와 소규모 그룹의 이름은 알콕시 치환기로 명명됩니다. 위에 주어진 예는 다음과 같습니다.
-
에 톡시 프로판 (에틸 프로필 에테르).
-
메 톡시 에탄 (메틸 에틸 에테르).
-
2- 메 톡시 -2- 메틸 프로판 (MTBE).
-
페녹시 벤젠 (디 페닐 에테르).
윌리엄슨 합성의 특성에 의한 에테르 준비
-
이것은 윌리엄슨의 합성으로도 알려진 에테르 (친 핵성 치환 반응)를 형성하는 가장 중요한 방법입니다. 그것은 알킬 할라이드의 알 옥사이드 이온에 의한 SN2 공격으로 구성됩니다. 알킬 설페이트 또는 알킬 설포 네이트.
친 핵성 치환 반응 (NA + C2H6- + C2H6CLC2H6OC2H6 + NA + CL-)
Willamson의 합성 메커니즘 :

에테르의 사용
-
디 에틸 에테르는 수술의 마취제로 사용됩니다.
-
에테르는 냉각제로 사용됩니다.
-
수지, 오일 등을 위해 업계에서 Grignard 시약 및 용매에서 반전 용매로 사용됩니다.
-
에테르는 휘발유와 함께 모터 연료로 사용됩니다.
-
페닐 에테르는 높은 비등점으로 인해 열 전달 매체로 사용할 수 있습니다.
결론 :
에테르는 두 개의 다른 또는 동일한 R 그룹에 부착 된 다음 분자 공식 R-O-R '중심 산소를 갖는 분자 또는 화합물이다. 산소에는 두 쌍의 고독한 전자가 있습니다. 에테르 화합물에 대한 명명법 시스템은 산소에 의해 결합되며 알파벳순으로 명명 된 다음 에테르라는 단어가 뒤 따른다. 3 개의 화합물 화합물 1은 다음 분자입니다. 동일한 이름 R 그룹과 디메틸이라는 두 개의 메틸기를 갖는 중심 산소가 있습니다. 에테르는 일반적으로 용매로 사용됩니다. 제품을 안정화시킬 수 있기 때문에 우수합니다.