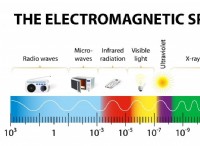
화염 착색은 미네랄 식별에 사용되는 방법입니다. 전자의 움직임이 금속의 색상을 유발하고 빛의 형태로 에너지를 방출한다는 원리에 기초합니다. 사용 된 금속에 따라이 빛의 색상이 변합니다. 더 큰 원자는 더 낮은 에너지로 색상을 방출하는 반면, 작은 원자는 더 큰 에너지로 색상을 생성합니다.
다양한 금속의 스펙트럼 라인은 뚜렷한 패턴을 가지며, 또한 다른 불꽃 색상을 형성하는 이유 중 하나이기도합니다.
화염 색상 중요성
과학자들은 화염 착색을 사용하여 알려지지 않은 화합물의 성분을 식별합니다. 이 정보는 분자를 식별하고 메탈 로이드 또는 금속 이온이 포함되어 있는지 결정하는 데 도움이됩니다.
불꽃의 원점
전자를 원자 또는 이온의 낮은 궤도에서 고온으로 가열하여 전자를 더 높은 궤도로 이동할 수 있습니다. 그들은 낮은 수준 (한 번에 또는 일정 기간)으로 떨어질 때 빛의 형태로 에너지를 방출합니다. 이러한 각 점프는 주어진 파장 (또는 주파수)에서 일정량의 에너지를 광 에너지로 방출합니다. 이러한 점프는 스펙트럼의 선을 형성하며, 그 중 일부는 보입니다. 색상의 혼합으로 구성됩니다.
나트륨 (또는 다른 금속) 이온의 높은 에너지는 눈이 볼 수없는 UV 스펙트럼의 선을 유발합니다. 전자는 금속 원자에서 더 높은 수준에서 하위 레벨에서 떨어지므로 화염 테스트에서 볼 수있는 점프가 발생합니다. 염화나트륨을 화염에 넣으면 특정 나트륨 이온은 전자를 얻고 가열 될 때 중성 나트륨 원자가됩니다. 비판적 상태에있는 나트륨 원자의 구조는 1S22S22P63S1이지만 화염 내에 몇 가지 흥분된 전자 상태가있을 것입니다. 프로모션 된 전자는 3p1 레벨에서 일반 3S 레벨로 떨어지면서 나트륨의 불꽃이 밝은 주황색 노란색을 제공합니다.
에너지 점프의 크기는 금속마다 다릅니다. 이는 각 금속이 고유 한 스펙트럼 라인 패턴을 가지므로 독특한 불꽃 색상을 가지고 있음을 의미합니다. 금속 이온에서의 전자의 움직임은 화염 색상을 생성하며 전자 구성 1S22S22P6이 있습니다. 불꽃은 전자를 가열하여 더 많은 에너지를 줄 수 있습니다. 전자가 화염에서 얻는 에너지의 양에 따라 7S 또는 6P 또는 4D와 같은 더 높은 궤도로 이동할 수 있습니다. 전자의 더 높고 불안정한 상태는 원래 상태로 되돌아 가지만 반드시 한 번의 전환은 아닙니다.
일반적인 화염 색상 예제는 무엇입니까?
나트륨은 노란색 불꽃, 리튬 및 스트론튬을 생성합니다. 빨간색 불꽃, 칼슘 오렌지 불꽃, 구리 푸른 불꽃 및 바륨 녹색 불꽃이 불꽃의 예입니다.
화염 테스트는 무엇입니까?
화염 테스트는 화학의 일반적인 분석 방법이며 화학 물질 또는 소금에서 성분을 감지하고 식별합니다. 화염 테스트는 화합물의 금속 이온을 감지하고 각 요소의 이온은 방출 스펙트럼에 따라 다른 기능을 가지고 있으므로 화염 테스트가 다릅니다.
불타는 금속 이온 소금 이이 차이를 보여줄 때 생성 된 화염의 색상. 각 요소의 방출 스펙트럼에는 이온이 아닌 원자가 포함됩니다. 화염 테스트에서 볼 수있는 컬러 라인은 이온으로 전환되는 전자로 인한 것입니다.
화염 테스트 뒤의 화학
화염 테스트 화학은 간단합니다. 우리가 원자 또는 이온을 고온으로 가열하면 전자는 정상 또는지면 상태 궤도보다 더 많은 에너지를 함유하는 일반 전략적 상태에서 더 높은 궤도로 홍보합니다.
이 흥분된 전자가 낮은 수준으로 돌아올 때 방출되는 에너지는 동시에 또는 단계로 발생할 수 있으며,이 에너지는 빛으로 방출됩니다.
각 도약은 정해진 수량의 광 에너지를 방출하고 각 궤도 전이는 주파수 또는 파장에 해당합니다.
이러한 전환 또는 점프는 스펙트럼의 선을 만듭니다. 이 라인은 스펙트럼에 나타납니다.
우리가 보는 마지막 색상은이 모든 색상이 혼합되어 있으며 불꽃 테스트에서 볼 수있는 요소의 독특한 색상입니다.
예를 들어, 전자 전이는 칼륨, 나트륨 및 기타 여러 금속 이온의 매우 높은 에너지에서 발생하여 UV 스펙트럼의 인간 눈에는 라인이 보이지 않습니다. 화염 테스트에서 이온이 아닌 원자가 사용되는 이유를 설명합니다.
금속 원자의 전자는 높은 수준에서 하위 수준에서 하위로 떨어지므로 화염 테스트가 점프됩니다. 나트륨 이온을 함유하는 염화나트륨이 고온으로 가열되면 일부 이온은 전자를 회복하고 중성 나트륨 원자를 형성합니다. 각 요소의 궤도 및 구성은 화염 테스트에서 중요한 기능입니다.
발전되지 않은 나트륨 원자 1S22S22P63S1 및 화염 내의 여기 전자 상태. 나트륨은 주황색 노란색 불꽃을 생성하며 전자를 정상 3S1 레벨로 다시 홍보 할 때 발생합니다.
잠재적 에너지 점프의 크기는 금속마다 다릅니다. 각 금속에는 고유 한 스펙트럼 라인 패턴이 있으므로 독특한 불꽃 색상이 있습니다.
그룹 1 금속은 화염 테스트를 사용하여 식별하기가 가장 쉽습니다. 화염 테스트는 가능한 화합물에 대한 아이디어를 제공하며 다른 금속에 대한 결정적인 식별이 아닙니다.
화염 테스트의 한계
- 이온의 농도가 낮은 한 화염 테스트는 그것들을 감지하지 못할 것입니다.
- 광 강도는 샘플마다 다릅니다. 예를 들어, 황색 나트륨 배출은 화염 테스트 중에 적색 리트머스 배출량보다 실질적으로 더 강렬합니다.
- 샘플에서 오염 물질 또는 불순물의 존재는 화염 테스트에 영향을 미칩니다. 예를 들어, 나트륨은 대부분의 화합물에 존재하며 불꽃 노란색을 제공합니다.
- 화염 테스트는 모든 요소를 구별 할 수 없습니다. 대부분의 금속은 비슷한 색상을 만들고 다른 화합물은 색상 변화가 없습니다.
결론
화학에서 가장 많이 사용되는 분석 기술 중 하나는 화염 색상 테스트입니다. 소금이나 화합물에서 특정 성분의 존재를 탐지하고 분석하는 인기있는 방법입니다. 화염 테스트는 화합물에서 금속 이온의 존재를 결정하며, 각 요소의 이온은 방출 스펙트럼에 기초하여 독특한 특징을 갖기 때문에 각 요소에 대한 화염 테스트는 다릅니다. 소금 함유 특정 금속 이온을 태울 때 생성 된 화염의 색은 이러한 구별을 보여줍니다. 각 요소의 방출 스펙트럼은 이온이 아닌 불꽃 색상을 결정한다는 점은 주목할 가치가 있습니다. 화염 테스트에서 보이는 가시적 인 색상 선은 원자에서 전자의 전이 때문입니다.