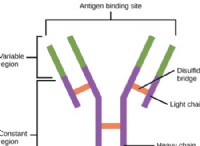
주요 차이 - 대착 대 밀도
농도와 밀도는 모두“물질의 양”의 지표입니다. 주요 차이 농도와 밀도 사이에는 농도가 혼합물에 얼마나 많은 물질이 존재하는지를 나타냅니다. , 밀도는 단위 부피당 물질의 질량을 나타냅니다 .
농도는 무엇입니까
농도는 혼합물에 물질이 얼마나 많이 존재하는지를 나타냅니다. 전형적으로, 이것은 혼합물의 부피로 표현된다. 예를 들어,
질량 농도 혼합물의 단위 부피에서 물질이 얼마나 많은 질량을 설명하는지를 제공합니다. 이것은 물질의 질량을 혼합물의 총 부피로 나눌 수 있습니다. 예를 들어, 5.00 g의 순수 테이블 소금 (NaCl)을 물에 용해시키기 위해 100cm의 소금 용액을 얻는다면 농도 용액의 소금은 5o.0 kg m입니다. 일반적으로 화학 실험에서 농도는 g cm에서 발현됩니다.
어금니 농도 몰의 수를 제공합니다 혼합물의 단위 부피당 물질. 예를 들어, 위에서 설명한 소금 솔루션을 사용해 보겠습니다. NaCl의 두더지의 질량은 58.5g입니다. 이는 상기 용액의 경우 1m의 용액 당 855 몰이 있어야한다는 것을 의미합니다. 따라서, 농도는 855 mol m으로 설명 될 수있다. 일반적으로 화학자는 특히 가스 농도를 논의 할 때 Mol DM 단위를 사용합니다. 리터당 두더지는 종종 상징 M으로 주어진다. HCl의 2m 용액은 1 L의 용액에 용해 된 2 몰의 HCl을 갖는다.
.볼륨 농도 솔루션의 양이 물질에 의해 점유되는 양을 제공합니다. 이것은 백분율로 표현 될 수 있습니다. 비율은 또한 질량의 양을 표현하는 데 사용됩니다. 물질에 의해 해결책을 설명합니다. 예를 들어, 1% 포도당 용액은 1 g의 포도당이 99g의 물에 용해 된 것을 갖는다.
종종 농도는 백만 (ppm) 당 부품으로도 주어집니다. 또는 10 억 (PPB) . 이러한 유형의 측정은 혼합물의 백만/10 억 분자 당 얼마나 많은 물질의 분자가 존재하는지를 나타냅니다. 예를 들어, 아래 그래프는 우리 대기에서 이산화탄소의 농도가 지난 수십 년 동안 어떻게 증가했는지를 보여줍니다.
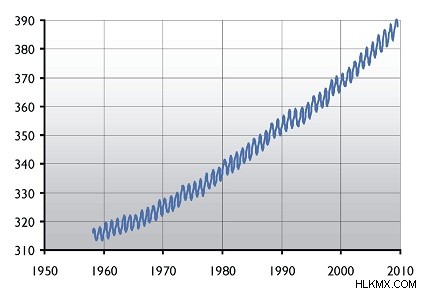
대기에서 이산화탄소의 변화, y 축에 표시된 백만 부분과 x 축
에 표시된 해의 농도가 농도입니다.단어 집중된 및 희석 종종 용액의 상대 농도를 나타내는 데 사용됩니다. 여기에서, 농축 희석 반면 더 높은 농도를 나타냅니다 낮은 농도를 나타냅니다.
밀도
아이들은 종종 서로를 수수께끼로 포즈를 취합니다.“ 더 무겁는 것은 무엇입니까? 1 파운드의 철 또는 깃털 파운드? 물론 그들은 모두 동일합니다! 그러나 직관적으로, 우리는 철이 무겁다 고 생각할 수 있습니다. 우리는 종종 비슷한 볼륨을 그림으로 비교하고 비교하기 때문입니다 우리의 마음에 철과 깃털의. 철은 밀도이기 때문에 , 우리는 그것이 더 많은 무게를 가져야한다고 생각합니다.
물질의 밀도는 단위량 당 질량을 나타냅니다 . 입방 미터의 철분은 깃털의 입방 미터보다 더 많은 질량을 가지고 있습니다. 철은 실온에서 약 7900kg m의 밀도를 가지며 물의 밀도는 약 1000kg m입니다. 깃털의 밀도는 약 2.5kg m입니다. 밀도는 부유 의 중요한 개념입니다 . 유체보다 밀도가 큰 경우 물질은 유체로 가라 앉습니다. 사해의 물은 너무 조밀합니다 , 사람은 단순히 떠 다닐 수 있습니다.

사해에 떠 다니는 남자
농도와 밀도의 차이
측정하는 것
농도 혼합물에 얼마나 많은 물질이 존재하는지 측정합니다.
밀도 단위 부피당 재료의 질량을 측정합니다.
다른 유형의 상호 작용
농도 반응물의 화학 반응 속도를 결정하는 데 중요한 요소입니다. 그러나 화학 반응을 겪지 않고 물질이 육체적으로 상호 작용할 때 농도는 덜 중요한 요소입니다.
밀도 반응 속도를 결정할 때는 반응물 (온도와 압력이 동일하다면 변하지 않음)은 덜 중요합니다. 그러나 밀도는 화학 결합이 파손되지 않은 물리적 상호 작용의 중요한 요소입니다.
다른 화합물의 존재
농도 에 대해 말하는 것은 의미가 없습니다 혼합물이 없을 때. 예를 들어, 요소의 농도에 대해 이야기하는 것은 의미가 없습니다.
밀도 물질을 특성화하는 데 사용될 수있는 속성입니다.