주요 차이 - 삼투압 대 삼투압
삼투압은 유체와 관련된 용어입니다. 삼투를 피하는 데 필요한 압력입니다. 다시 말해, 삼투압은 삼투를 통해 용해 된 용질을 갖는 용액으로 들어가는 순수한 용액을 피하기 위해 적용되어야하는 압력이다. 삼투압과 삼투압은 삼투압에 연결됩니다. 그들은 삼투압 측면에서 삼투압을 측정하는 데 사용됩니다. Osmole은 삼투압에 기여하는 화합물의 두더지 수입니다. 삼투압과 삼투압의 주요 차이점은 삼투압이 용액의 부피를 고려하는 척도이며, 용액의 질량을 고려하여 삼투압이 측정된다는 것입니다.
주요 영역이 적용됩니다
1. 삼투압
- 정의, 예제에 대한 설명
2. 삼투압이란?
- 정의, 예제에 대한 설명
3. 삼투압과 삼투압의 관계는 무엇입니까
- 방정식의 설명
4. 삼투압과 삼투압의 차이는 무엇입니까
- 주요 차이점 비교
주요 용어 :삼투압, 삼투압, 삼투압, 삼투압 
삼투압이란 무엇입니까
삼투압은 고려중인 솔루션의 리터당 OSMOLES 수입니다. 다시 말해, 삼투 활성을 나타내는 용액의 농도를 표현하는 데 사용되는 용어입니다. 이것은 삼투압이 삼투압의 농도임을 의미합니다. 이것을 삼투 농도라고도합니다.
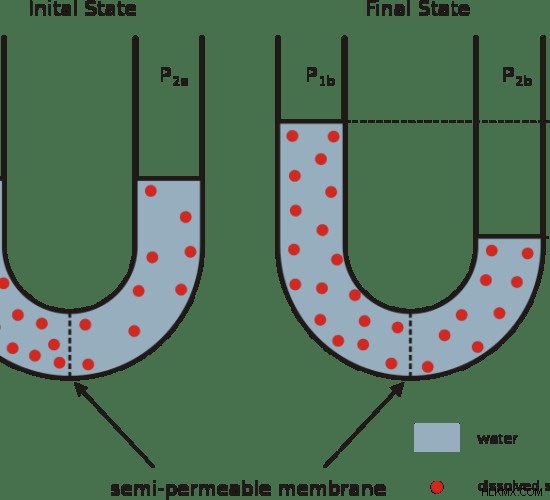
그림 1 :삼투증
어금니와 달리 삼투압은 리터당 입자 수를 측정합니다. 예를 들어, NaCl 용액을 고려하면 삼투압은 해당 솔루션의 몰토리보다 두 배나 주어집니다. 이는 몰로성이 리터당 Na 또는 Cl 몰의 수이기 때문에 삼투압은 모든 입자가 고려되기 때문에 리터당 (Na+Cl) 두더지이기 때문입니다.
우리가 이온 성 화합물의 용액을 고려하면 모든 이온은 특정 이온이 아닌 입자로 간주됩니다. 입자는 이온 또는 분자 일 수 있습니다. 그러나 분자 구조를 갖는 화합물의 용액을 고려하면 화합물은 분자를 용해시킬 것이다. 그런 다음 각 분자는 입자로 간주됩니다.
예를 들어,
- 0.08 몰의 포도당이 1 리터의 물에 용해 된 경우;
포도당 용액의 몰토리성 =0.08 mol/l
포도당 용액의 삼투압 =0.08 Osmol/L
- 0.08 몰의 NaCl이 1 리터의 물에 용해 된 경우;
NaCl 용액의 몰토리성 =0.08 mol/l
NaCl 용액의 삼투압 =0.16 Osmol/L
삼투압은 용액에 용해 된 화합물의 유형에 의존하지 않습니다. 그것은 단지 존재하는 입자의 양을 측정합니다. 그러나 그것은 용매 (물)의 변화에 영향을받습니다. 용액의 부피가 증가하거나 감소하면 삼투압 계산을 위해 고려되는 부피가 그에 따라 변경되기 때문입니다. 또한 삼투압은 또한 온도와 압력에 의존합니다. 화합물의 부피와 용해도는 해당 매개 변수를 변경하여 변경 될 수 있기 때문입니다.
.osmolality
삼투압은 용액 질량에 관한 용액의 삼투압을 설명하는 데 사용되는 용어입니다. 솔루션의 1 킬로그램 당 Osmoles의 수로 정의 될 수 있습니다. 삼투는 해당 용액에 존재하는 입자의 몰입니다. 입자는 이온 또는 분자 일 수 있습니다.
질량은 압력과 온도와 무관 하므로이 두 매개 변수는 용액의 삼투압에 영향을 줄 수 없습니다. 그러나 수분 함량의 변화는 용액의 질량을 변화시키기 때문에 삼투압에 큰 영향을 줄 수 있습니다. 이 특성은 모든 온도 및 압력 조건에서 삼투압을 정확하게 결정하는 데 유리합니다.
osmolality는 동결 지점 우울증 방법에 의해 쉽게 결정될 수 있습니다. 그것은 용질의 간접 비례와 용액의 동결 지점을 기반으로합니다 (용액의 용질이 많을수록 하위가 얼어 붙습니다)
.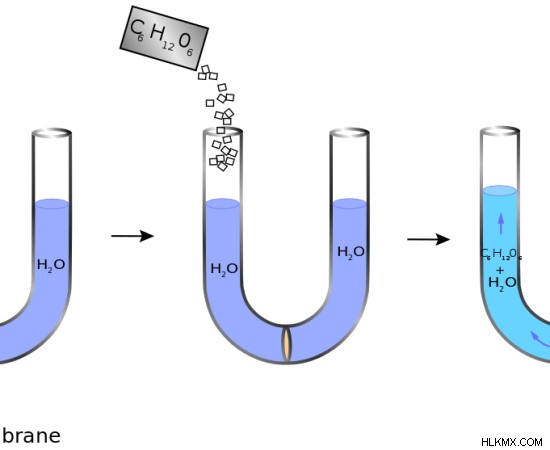
그림 2 :화합물이 물에 용해 될 때 삼투압이 발생합니다.
삼투압의 단위는 Osmol/kg입니다. 삼투압은 용액의 질량 측면에서 용액에서 용질의 농도를 제공합니다.
삼투압과 삼투압의 관계
- 매우 희석 된 용액의 경우 삼투압과 삼투압은 수치 적으로 동일합니다.
- 삼투압과 삼투압의 차이를 삼투압 갭이라고합니다.
삼투압과 삼투압의 차이
정의
삼투압 : 삼투압은 용액 리터당 용질 입자의 삼투압으로 표현 된 용액의 농도입니다.
삼투압 : 삼투압은 킬로그램 당 용질 입자의 총 수로 표현 된 용액의 농도입니다.
계산
삼투압 : 삼투압은 용액의 부피를 고려하여 계산됩니다.
삼투압 : 삼투압은 용액의 질량을 고려하여 계산됩니다
단위
삼투압 : 삼투압의 단위는 mol/l입니다.
삼투압 : 삼투압 유닛은 Osmol/L입니다.
온도 및 압력
삼투압 : 삼투압은 온도와 압력에 따라 다릅니다.
삼투압 : 삼투압은 온도와 압력에 의존하지 않습니다.
결론
삼투압과 삼투압은 시스템의 삼투압을 결정하는 데 사용됩니다. 그들은 삼투압 측면에서 용액의 농도를 설명합니다. 그러나이 기사에서 위에서 논의한 바와 같이 몇 가지 차이가 있습니다. 삼투압과 삼투압의 주요 차이점은 용액의 부피를 고려하여 삼투압이 측정되는 반면, 용액의 질량을 고려하여 삼투압이 측정된다는 것입니다.
.