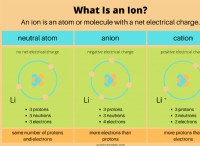
산이 염기와 반응 할 때, 산으로부터의 수소 (H+) 이온은 염기로부터 수산화물 (OH-) 이온과 결합하여 물 (H2O)을 형성한다. 염기로부터 나머지 전하 이온 (양이온)과 산으로부터 음으로 하전 된 이온 (음이온)은 염을 형성한다.
예를 들어, 염산 (HCL)이 수산화 나트륨 (NAOH)과 반응 할 때, 생성물은 물과 염화나트륨 (NaCl)이다. 나트륨 및 염화물 이온은 소금을 형성하는 반면, 수소 및 수산화물 이온은 물을 형성하기 위해 결합된다.
$$ \ text {hcl (aq)} + \ text {naoh (aq)} → \ text {h} _2 \ text {o (l)} + \ text {naCl (aq)} $$
이 경우, 생성 된 용액은 물에 용해 된 염화나트륨을 함유하고 있기 때문에 바닷물이 될 것이다. 그러나, 산-염기 반응이 염화나트륨을 생성하지 않는 상이한 반응물을 포함하는 경우, 생성 된 용액은 바닷물이되지 않을 것이다. 예를 들어, 황산 (H2SO4)과 수산화 칼륨 (KOH)과 반응하는 것은 물과 황산 칼륨 (K2SO4)을 생성하지만 염화나트륨 형성이 없기 때문에 바닷물은 생성되지 않을 것이다.
$$ \ text {h} _2 \ text {so} _4 (\ text {aq}) + 2 \ text {koh} (\ text {aq}) → \ text {2h} _2 \ text {o (l)} + \ text {k} _2 \ text {so} _4 \ text {(aq)} $$
따라서, 산-염기 반응은 염 및 물을 생성 할 수 있지만, 결과 용액은 반응이 염화나트륨의 형성과 관련된 경우에만 바닷물 일 것이다.