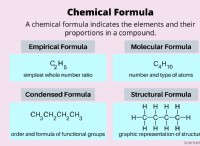
1. 구조 이성질체 :
* 원자의 다른 배열 : 동일한 공식이지만 원자의 다른 배열을 구조 이성질체라고합니다. 이러한 구조의 차이는 상이한 화학적 특성과 반응성으로 이어진다. 예를 들어, 부탄 (C4H10)은 2 개의 구조 이성질체 인 N- 부탄 및 이소 부탄으로서 존재한다. 그들은 뚜렷한 모양으로 인해 끓는점과 반응성이 다릅니다.
2. 입체 이성질체 :
* 다른 공간 배열 : 입체 이성질체는 동일한 구조적 공식을 가지지 만 원자의 3 차원 배열은 다릅니다. 이 차이는 다음과 같이 발생할 수 있습니다.
* 거울상 이성질체 : 왼쪽과 오른손과 같은 감독 불가능한 거울 이미지. 그들은 종종 생물학적 시스템의 효소와 같은 키랄 환경과 다른 상호 작용을 나타냅니다.
* diastereomer : 서로의 이미지가 아닌 입체 이성질체. 그들은 물리적, 화학적 특성이 다릅니다.
3. 기능적 그룹 이성질체 :
* 다른 기능 그룹 : 동일한 공식을 갖는 분자는 다른 기능 그룹이 부착 될 수 있습니다. 기능적 그룹은 분자의 반응성에 영향을 미치는 원자의 특정 배열이다. 예를 들어, 에탄올 (C2H5OH) 및 디메틸 에테르 (CH3OCH3) 둘 다 포뮬러 C2H6O를 가지지 만 기능 그룹 (에탄올 대 디메틸 에테르의 에테르 연계에서의 하이드 록실 그룹)에서는 상이하여 별개의 화학적 거동을 초래한다.
4. 형태 이성질체 :
* 단일 본드 주변의 다른 회전 : 구조적 이성질체는 단일 결합 주위의 회전에 의해 상호 연결 될 수있는 분자의 상이한 공간 배열이다. 이들 순응자는 종종 다른 에너지를 가지며, 특히 Steric 방해와 관련된 반응에서 반응성에 영향을 줄 수있다.
5. 동성상 :
* 양성자 전달을 통한 상호 전환 : 타우토머는 양성자의 움직임을 통해 상호 연결되는 이성질체이다. 이러한 다른 형태는 평형에 존재할 수 있으며, 이는 상이한 반응성을 초래한다.
요약하면, 두 분자는 동일한 화학적 공식을 갖지만, 다른 구조, 공간 배열, 기능 그룹 또는 동적 상호 연결은 화학적 거동과 반응에 상당한 차이를 초래할 수 있습니다.