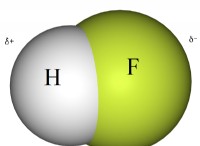
다음은 고장입니다.
* 양성자 : 이들은 수소 이온 (H+)이다.
* 기부 : 산은 다른 분자에 양성자를 제공한다.
Brønsted-lowry 산의 주요 특성 :
* 그들은 이온화 될 수있는 적어도 하나의 수소 원자를 함유하고 (양성자로 방출)
* 그들은 용액에서 H+ 이온의 농도를 증가시킵니다.
* 그들은 컨쥬 게이트 염기와 컨쥬 게이트 산을 형성하기 위해 염기와 반응합니다. .
Brønsted-lowry 산의 예 :
* 염산 (HCl) : HCl → H++ Cl- (H+ 및 Cl-를 형성하기 위해 양성자를 기증합니다)
* 아세트산 (CH3COOH) : CH3COOH → H++ CH3COO- (H+ 및 아세테이트 이온을 형성하기 위해 양성자를 기증합니다)
* 황산 (H2SO4) : H2SO4 → H++ HSO4- (H+ 및 바이 설페이트 이온을 형성하기 위해 양성자를 기증합니다)
중요한 참고 :
* Brønsted-Lowry 이론은 Arrhenius 이론에 비해 산과 염기에 대한보다 포괄적 인 정의입니다. 정의를 수용액으로 제한하지 않으며 다른 용매에서 양성자 전달 반응을 포함하도록 개념을 확장합니다.