기본 이해
* 혼합물 : 물리적으로 결합되었지만 화학적으로 결합되지 않은 둘 이상의 물질의 조합. 그들은 육체적 수단으로 분리 될 수 있습니다.
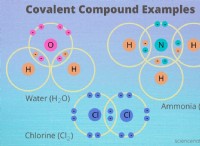
* 화합물 : 둘 이상의 원소는 고정 비율로 화학적으로 결합되었습니다. 그들은 구성 요소와 구별되는 새로운 특성을 가지고 있으며 화학 반응에 의해서만 분리 될 수 있습니다.
차이를 식별하기위한 절차
1. 육안 검사 :
* 혼합물 : 종종 모래와 물, 기름과 물과 같은 이질적인 외관 (다른 부분이 보이는)이 있습니다.
* 화합물 : 물에 용해 된 소금과 같은 균질 한 (전체적으로 균일).
2. 분리 기술 :
* 혼합물 : 다음과 같은 물리적 수단으로 분리 될 수 있습니다.
* 여과 : 액체에서 고체를 분리 (예 :물에서 모래).
* 증발 : 액체로부터 용해 된 고체를 분리 (예 :물에서 소금).
* 증류 : 끓는점 (예 :물에서 에탄올)에 기초한 액체 분리.
* 자기 : 비자 성 물질로부터 자기 재료를 분리하는 (예 :모래에서 철제 제출).
* 화합물 : 물리적 수단으로 분리 될 수 없습니다. 그들은 결합을 깨기 위해 화학 반응이 필요합니다.
3. 속성 :
* 혼합물 : 구성 요소는 원래 특성을 유지합니다. 예를 들어, 철 파일과 모래의 혼합물에서 철과 모래는 개별 자기 및 화학적 특성을 유지합니다.
* 화합물 : 이 화합물은 구성 요소와 구별되는 새로운 특성을 갖는다. 예를 들어, 물 (HATE)은 수소 (HAT) 및 산소 (O₂)와 비교하여 상이한 끓는점, 밀도 및 화학 반응성을 갖는 액체이다.
4. 구성 :
* 혼합물 : 구성 요소의 비율은 다를 수 있습니다. 소금과 물을 다른 양의 소금으로 혼합 할 수 있습니다.
* 화합물 : 요소의 비율은 고정되고 일정합니다. 물은 항상 수소 대 산소 원자의 2 :1 비율을 갖는다.
예
* 혼합물 : 소금과 후추, 공기, 모래 및 물.
* 화합물 : 물 (HATER), 테이블 소금 (NaCl), 이산화탄소 (CO₂).
키 포인트
* 화학 결합 : 이것이 결정적인 차이입니다. 혼합물은 화학적 결합이 부족합니다. 화합물에는 그것을 가지고 있습니다.
* 분리 : 물리적 방법은 혼합물에서 작동합니다. 화합물에는 화학적 방법이 필요합니다.
* 속성 : 혼합물은 원래 특성을 유지합니다. 화합물에는 새로운 특성이 있습니다.
더 많은 예제 나 설명을 원하시면 알려주세요!