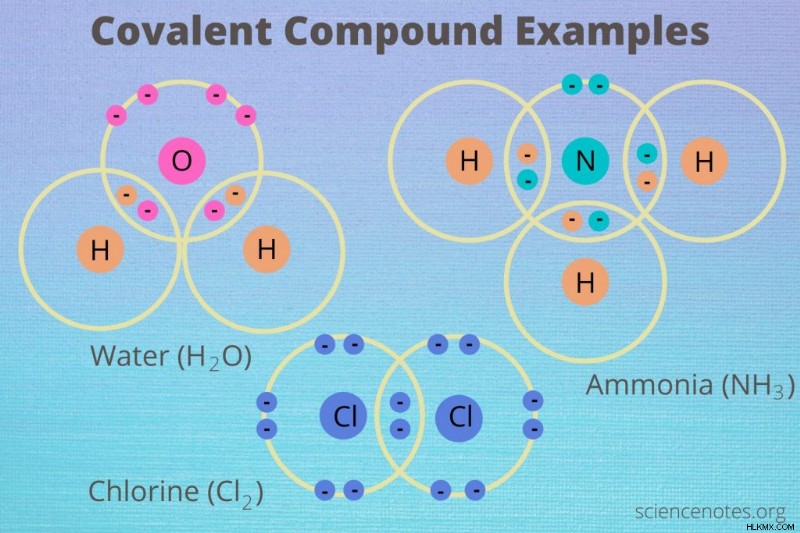
공유 화합물 또는 분자 화합물은 공유 결합에 의해 연결된 원소로 제조 된 화학적 화합물이다. 공유 결합은 이들 요소가 동일하거나 유사한 전기 음성 값을 가지기 때문에 비금속 원소 사이에만 형성됩니다. 다음은 공유 화합물의 예와 공통 특성을 살펴 봅니다.
공유 화합물의 예
공유 화합물은 비금속으로 만 구성되므로 인식 할 수 있습니다. 또는 전기 음성 값 표를 참조하십시오. 화합물에서 요소의 전기 음성 값이 동일하거나 유사한 경우, 공유 화합물을 형성합니다. 일반적으로 전기 음성 차이가 폴링 스케일에서 2 미만인 경우, 원자는 공유 결합을 형성합니다. 전기 음성 차이가 2 이상인 경우 원소는 이온 결합을 형성합니다.
공유 화합물의 예는 다음과 같습니다.
- o 2 - 산소
- cl 2 - 염소
- pcl 3 - 인 트리클로라이드 인
- ch 3 ch 2 오 - 에탄올
- o 3 - 오존
- h 2 - 수소
- h 2 O - 물
- HCL - 수소 염화수소
- ch 4 - 메탄
- nh 3 - 암모니아
- co 2 - 이산화탄소
- 단백질
- 탄수화물 (설탕과 전분)
- 지질 (지방)
- 핵산 (DNA 및 RNA)
유기 화합물은 모두 공유 화합물입니다.
규칙에 대한 예외
일반적으로 분자가 전적으로 비금속으로 구성된 경우 공유 화합물이라고 가정 할 수 있습니다. 그러나 주목할만한 예외가 있습니다. 암모늄 양이온 (NH <서브> 4 )는 전기 양성이므로 공유 결합보다는 비금속과 이온 결합을 형성합니다. 동시에, 질소와 수소 원자 사이의 결합은 공유이다. 따라서 염화 암모늄과 같은 화합물 (NH <서브> 4 Cl) 및 질산 암모늄 (NH <서브> 4 아니오
공유 화합물 특성
공유 화합물은 몇 가지 공통 특성을 공유합니다.
- 낮은 용융점
- 낮은 비등 지점
- 가난한 전기 도체
- 열악한 열 도체
- 부서 지거나 부드러운 고형물을 형성합니다
- 퓨전의 낮은 엔탈피
- 기화의 낮은 엔탈피
융점이 낮기 때문에 많은 분자 화합물은 실온에서 액체 및 가스입니다. 고체 공유 화합물은 공유 결합 (때로는 수소 결합)이 상대적으로 파손되기 때문에 부드럽거나 부서지기 쉬운 경향이 있습니다. 화합물 내의 공유 전자는 전자 이동성을 제한하므로 공유 화합물은 이온 성 화합물뿐만 아니라 열이나 전기를 전도하지 않습니다.
이온 성 및 공유 화합물 식별 실습

워크 시트를 사용하여 공유 화합물을 얼마나 잘 이해하는지 테스트하십시오. 이 PDF 워크 시트 및 답변 키를 다운로드하여 인쇄하여 화합물의 이름을 묻고 이온 성인 또는 공유인지
[ PDF 워크 시트 ] [ 답변 키 ]
참조
- Campbell, Neil A.; 윌리엄슨, 브래드; Heyden, Robin J. (2006). 생물학 :삶 탐험 . 보스턴, MA :Pearson Prentice Hall. ISBN 0-13-250882-6.
- 3 월, Jerry (1992). 고급 유기 화학 :반응, 메커니즘 및 구조 . John Wiley &Sons. ISBN 0-471-60180-2.
- Tranks, D. R.; Heffernan, M.L.; Lee Dow, K. C.; McTigue, P. T.; Withers, G. R. A. (1970). 화학 :구조적 관점 . Carlton, Vic. :Melbourne University Press. ISBN 0-522-83988-6.