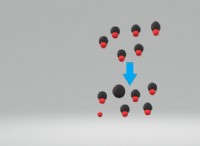
다음은 고장입니다.
가스 :
* 광범위한 간격 분자 : 가스 분자는 멀리 떨어져 있으며 그 사이에 큰 빈 공간이 있습니다.
* 약한 분자간 힘 : 가스 분자 사이의 매력은 매우 약합니다.
* 높은 압축성 : 가스에 압력을 가하면 분자가 더 가까워지면서 빈 공간이 줄어 듭니다. 이것이 바로 가스가 압축성이 높은 이유입니다.
액체 :
* 더 가까운 분자 : 액체 분자는 가스 분자보다 더 가깝지만 여전히 그 사이에 공간이 있습니다.
* 보통 분자간 힘 : 액체는 가스보다 더 강한 인력을 가지고 있지만 고체보다 약합니다.
* 보통 압축성 : 액체는 분자가 더 가깝고 분자간 힘이 더 강하기 때문에 가스보다 압축성이 떨어집니다. 그러나 고압 하에서 여전히 약간 압축 가능합니다.
고체 :
* 밀접하게 포장 된 분자 : 고체 분자는 그들 사이의 공간이 거의없고 단단히 포장됩니다.
* 강한 분자간 힘 : 고체는 세 가지 물질 상태의 가장 강력한 분자간 힘을 가지고 있습니다.
* 낮은 압축성 : 고체 분자는 엄격하게 제자리에 고정되어있어 더 가깝게 밀기가 매우 어렵습니다. 이것이 고체가 일반적으로 비압축성으로 간주되는 이유입니다.
요약 :
* 압축 물질의 능력은 분자 사이의 공간과 그들을 붙잡는 힘의 강도와 직접 관련이 있습니다.
* 가스는 가장 많은 공간과 가장 약한 힘을 가지므로 압축성이 가장 높습니다.
* 고체는 공간이 가장 적고 가장 강한 힘을 가지므로 압축성이 가장 적습니다.
* 액체는 그 사이 어딘가에 떨어집니다.