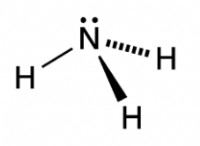
1. 원자가 전자 : 원자는 핵을 둘러싼 에너지 수준의 전자를 가지고 있습니다. 가장 바깥 쪽 레벨은 원자가 쉘이라고하며,이 쉘의 전자를 원자가 전자라고합니다. 이 전자는 화학적 결합에 관여합니다.
2. 공유 : 안정적인 전자 구성 (고귀한 가스와 같은)을 달성하기 위해, 원자는 전자를 얻거나 잃거나 공유하는 경향이 있습니다. 공유 결합에서, 원자 공유 원자가 전자가 가장 바깥 쪽 껍질을 채우는 전자.
3. 겹치는 궤도 : 두 원자가 서로 접근하면 원자가 전자 궤도가 겹치기 시작합니다. 이 중첩은 전자를 두 원자 사이에서 공유 할 수있게합니다.
4. 전자 쌍 : 공유 전자는 쌍 를 형성합니다 , 원자 궤도의 겹치는 영역에 존재한다. 이 공유 전자 쌍은 두 원자의 핵에 끌려되어 함께 붙잡 힙니다.
5. 공유 결합 유형 :
* 단일 본드 : 원자는 한 쌍의 전자 (예를 들어, 수소 분자에서 H-H)를 공유한다.
* 이중 채권 : 원자는 2 쌍의 전자를 공유합니다 (예 :산소 분자에서 O =O).
* 트리플 본드 : 원자는 3 쌍의 전자 (예를 들어, 질소 분자에서 N≡N)를 공유합니다.
공유 결합의 주요 특성 :
* 강한 채권 : 공유 결합은 상대적으로 강하기 때문에 상당한 에너지가 필요합니다.
* 방향성 : 공유 전자 쌍은 결합 된 원자 사이에 국한되어 공간의 특정 방향을 제공합니다.
* 비극성 및 극성 :
* 비극성 공유 결합 : 동일한 요소의 원자 또는 유사한 전기 음성 (전자를 유치하는 능력)을 갖는 원자 사이에서 발생합니다. 공유 전자는 동일하게 공유됩니다.
* 극성 공유 결합 : 전기성이 다른 원자 사이에서 발생합니다. 공유 전자는보다 전기 음성 원자를 향해 더 많이 끌어 와서 원자에 부분 양성 및 음전하를 만듭니다.
예 :
물 분자 (H₂O)의 형성을 고려하십시오.
* 산소 (O)는 6 개의 원자가 전자를 가지며 안정적인 옥셋을 달성하기 위해 2 개가 필요합니다.
* 수소 (H)는 1 개의 원자가 전자를 가지며 안정적인 듀엣을 달성하기 위해 1이 더 필요합니다.
산소는 각 수소 원자와 하나의 전자를 공유하여 2 개의 극성 공유 결합을 형성합니다. 각 수소 원자는 이제 두 개의 전자를 공유하여 듀엣을 완성하며 산소에는 8 개의 원자가 전자가있어 옥셋을 완성합니다.